
| A. | 液态氟化氢中存在氢键,所以其分子比氯化氢更稳定 | |
| B. | 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S | |
| C. | 邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键 | |
| D. | 若X+和Y2-的核外电子层结构相同,则原子序数:Y<X |
分析 A.氢化物的稳定性与非金属的非金属性强弱有关,与氢键无关;
B.元素最高价氧化物对应水化物的酸性越强,则非金属性越强;
C.邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛能够形成分子间氢键,分子内氢键要弱于分子间氢键;
D.若X+和Y2-的核外电子层结构相同,则X位于Y的下一个周期.
解答 解:A.氢化物的稳定性与非金属的非金属性强弱有关,与氢键无关,氢键影响氢化物的熔沸点,故A错误;
B.比较最高价氧化物对应水化物的酸性,才能比较非金属性,故B错误;
C、由于邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛能够形成分子间氢键,而分子内氢键要弱于分子间氢键,所以邻羟基苯甲醛比对羟基苯甲醛熔、沸点低,故C错误;
D.若X+和Y2-的核外电子层结构相同,电X位于Y的下一个周期,故原子序数Y<X,故D正确;
故选D.
点评 本题考查非金属元素性质的递变规律,为高频考点,题目难度中等,明确元素周期表结构、原子结构及元素周期律的关系是解本题关键,易错选项是A,注意氢键只影响氢化物的熔沸点,化学键影响物质稳定性,注意二者的区别.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )
.它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤④⑤② | B. | ③⑤② | C. | ③⑤①② | D. | ③⑤①⑤② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | 乙烯的燃烧:CH2=CH2+3O2$\stackrel{点燃}{→}$ 2CO2+2H2O | |
| C. | Fe2O3+6HCl═2FeCl3+3H2O | |
| D. | Na2CO3+H2O+CO2═2NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8gCH4含有5NA个电子 | |
| B. | 1mol Na与足量乙醇完全反应,失去2NA电子 | |
| C. | 1L 0.1mol•L-1的醋酸溶液中含有0.1NA个H+ | |
| D. | 标准状况下,22.4L苯含有约NA个C6H6分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氢原子的电子云图中,每个小黑点代表一个电子 | |
| B. | 某基态原子3d能级中电子排布的情况可能为 | |
| C. | 电子构型为[Ar]3d104s2的元素是过渡金属元素 | |
| D. | 当碳原子的核外电子排布由1s22s22p2转变为1s22s12p3时,碳原子由基态变为激发态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的电子式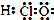 | |
| B. | 比例模型 :可以表示CH4,也可以表示CCl4 :可以表示CH4,也可以表示CCl4 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 碳酸氢根电离:HCO3-?H++CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com