
【题目】在一定条件下,C(s)+ H2O(g) ![]() CO+ H2(g)△H>0 在一容积固定的密闭容器中放入足量的焦炭与一定量的水蒸气进行反应,下列有关图像正确的是
CO+ H2(g)△H>0 在一容积固定的密闭容器中放入足量的焦炭与一定量的水蒸气进行反应,下列有关图像正确的是
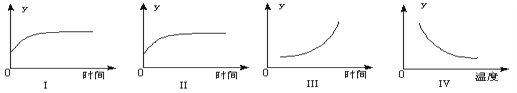
A. Ⅰ图表示反应进行过程中气体平均相对分子质量的变化
B. Ⅱ图表示反应进行过程中气体密度的变化
C. Ⅲ图表示反应达到平衡后,移去焦炭后水蒸气的百分含量的变化(忽略表面积的影响)
D. Ⅳ图表示反应达到平衡后,升高温度CO的百分含量的变化
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
(1)硫酸生产过程中2SO2(g)+O2(g)![]() 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据图回答下列问题:

①2SO2(g)+O2(g)![]() 2SO3(g)的△H__________0(填“>”或“<”),
2SO3(g)的△H__________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是_________。
a.体系的密度不发生变化 b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化 d.单位时间内反应物转移4 mol 电子,同时消耗2 mol SO3 e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g) ![]() 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

①升高温度,该反应的平衡常数__________(填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)=________,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为________(填“a”或“b”或“c”或“d”)。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 ______点,温度T1 ___T2(填“>”或“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 分子式符合Cn(H2O)m的,一定是糖类
B. 米酒变酸的过程涉及了氧化反应
C. 福尔马林是一种良好的杀毒剂,也可用来消毒自来水
D. 保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用品的主要成分不正确的是
A | B | C | D | |
用品 | 水玻璃 | “84”消毒液 | 食用纯碱 | 复方氢氧化铝片 |
主要成分 | Na2SiO3 | NaClO | NaHCO3 | Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是重要的化学试剂,化工原料和有广阔发展前景的新能源。
请回答下列问题:
I.实验室用锌和稀硫酸制备氢气时,可向稀硫酸中滴加少量硫酸铜溶液以加快反应速率,原因为____________。
II.以甲醇为原料制备氢气的一种原理如下:
i . CH3OH(g) ![]() CO(g)+2H2(g) △H=+90kJ·mol-1
CO(g)+2H2(g) △H=+90kJ·mol-1
ii. CO(g)+H2O(g)![]() CO2(g)+ H2(g) △H=-41kJ·mol-1
CO2(g)+ H2(g) △H=-41kJ·mol-1
(1)已知:断裂1 mol分子中的化学健需要吸收的能量如下表所示。

表中x =___________。
(2)向vL恒容密闭容器中充入lmo1 CH3OH(g),发生反应i,图l中能正确表示CH3OH(g)的平衡转化率(a)随温度(T)变化关系的曲线为________(填“A ”或“B”),理由为______,T1℃ 时,体系的平衡压强与起始压强之比为___________________。

(3)起始向10L恒容密闭容器中充入1 mol CH3OH(g)和1molH2O(g),发生反应i和反应ii,体系中CO的平衡体积分数与温度(T)和压强(p)的关系如图2所示。
①随着温度升高, ![]() 的值_______(填“增大”“ 减小” 或“不变”),理由为_____。
的值_______(填“增大”“ 减小” 或“不变”),理由为_____。
②P1、P2、p3由大到小的顺序为_______。
③测得C点时,体系中CO2的物质的量为0 . 2 mol,则T2℃时,反应ii的平衡常数K=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和O2的混合气体。在同温同压下,两容器内的气体一定不相同的( )
A.原子数 B.物质的量 C.密度 D.分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染问题越来越受到人们的关注,造成环境污染的主要原因是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是
A. 温室效应——CO2 B. 光化学污染——NO2
C. 酸雨——SO2 D. 臭氧层破坏——CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锰精矿是重要的银矿资源,其主要成分为MnO2和银单质,利用黄铁矿(主要成分为FeS2)可以实现锰和银的分离。具体操作流程如下:

(1)提高锰元素浸出率的措施(任写—条)___________。
(2)浸出1中,黄铁矿转化为铁盐和硫酸盐,请写出发生反应的化学方程式___________。
(3)从工业生产成本考虑,加入的A最好是______________。
A.CaCO3 B.NaOH C.氨水 D.Ca(OH)2
⑷浸出液2的主要成分Ag(CN)2-,写出浸出2中发生反应的离子方程式________;电解后的溶液中,可以循环利用的物质_______(填化学式)。
(5)如图可知,当液固比(水与矿料的质量比)大于5时,浸出率反而降低的原因________。

(6)银锰矿中,银矿物以显微粒状分散在MnO2矿物中,不破坏原有结构难以提银,因此锰的浸出对于银的提取率至关重要。某小组通过实验,研究了硫酸用量、黄铁矿用量(占矿重百分比)对锰浸出率的影响,如表所示:
硫酸% | 31.52 | 36.10 | 40.67 | 45.25 |
锰浸出率 | 77.42 | 89.49 | 91.59 | 97.95 |
黄铁矿% | 12.5 | 15 | 17.5 | 20 |
锰浸出率 | 88.79 | 97.95 | 99.18 | 99.46 |
从实际生产角度出发,下表中所给浸出条件最佳的是________。
A | 硫酸45.25% | B | 硫酸31.52% | C | 硫酸45.25% | D | 硫酸36.10% |
黄铁矿20% | 黄铁矿15% | 黄铁矿15% | 黄铁矿20% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com