
| A£® | ¢Ł¢Ś¢Ż | B£® | ¢Ł¢Ū¢Ž | C£® | ¢Ś¢Ü¢Ż | D£® | ¢Ł¢Ś¢Ü |
·ÖĪö ¢ŁĪŽÉ«ČÜŅŗÖŠ²»ŗ¬ÓŠÉ«Ąė×ÓĢśĄė×Ó”¢øßĆĢĖįøłĄė×Ó£»
¢ŚpH=11µÄČÜŅŗ³Ź¼īŠŌ£»
¢Ū¼ÓČėAlÄܷųöH2µÄČÜŅŗĪŖĒæ¼īČÜŅŗ»ņ·ĒĒæŃõ»ÆŠŌĖįČÜŅŗ£»
¢ÜÓÉĖ®µēĄė³öµÄc£ØOH-£©=10-13mol•L-1µÄČÜŅŗ³ŹĖįŠŌ»ņ¼īŠŌ£»
¢ŻÄÜŹ¹pHŹŌÖ½±äĪŖĄ¶É«µÄČÜŅŗĪŖ¼īŠŌČÜŅŗ£¬ĖÄÖÖĄė×ÓÖ®¼ä²»·“Ó¦£¬¶¼²»ÓėĒāŃõøłĄė×Ó·“Ó¦£»
¢ŽĖįŠŌČÜŅŗÖŠ²»ĻõĖįøłĄė×ÓÄܹ»Ńõ»ÆµāĄė×Ó£®
½ā“š ½ā£ŗ¢ŁCu2+”¢MnO4-ĪŖÓŠÉ«Ąė×Ó£¬ŌŚČÜŅŗÖŠ²»ÄÜ“óĮæ¹²“ę£¬¹Ź¢Ł“ķĪó£»
¢ŚpH=11µÄČÜŅŗ³Ź¼īŠŌ£¬CO32-”¢Na+”¢AlO2-”¢NO3-Ö®¼ä²»·“Ó¦£¬¶¼²»ÓėĒāŃõøłĄė×Ó·“Ó¦£¬ĖłŅŌÄÜ“óĮæ¹²“ę£¬¹Ź¢ŚÕżČ·£»
¢Ū¼ÓČėAlÄܷųöH2µÄČÜŅŗĪŖĒæ¼īČÜŅŗ»ņ·ĒĒæŃõ»ÆŠŌĖįČÜŅŗ£¬ĖįŠŌ»ņ¼īŠŌĢõ¼žĻĀ¶¼²»ÄÜ“óĮæ“ęŌŚHCO3-£¬¼īŠŌĢõ¼žĻĀ²»ÄÜ“óĮæ“ęŌŚNH4+£¬¹Ź¢Ū“ķĪó£»
¢ÜÓÉĖ®µēĄė³öµÄc£ØOH-£©=10-13mol•L-1µÄČÜŅŗ³ŹĒæĖįŠŌ»ņĒæ¼īŠŌ£¬Na+”¢Ba2+”¢Cl-”¢I- Ö®¼ä²»·“Ó¦ĒŅŗĶĒāĄė×Ó»ņĒāŃõøłĄė×Ó¶¼²»·“Ó¦£¬ĖłŅŌÄÜ“óĮæ¹²“ę£¬¹Ź¢ÜÕżČ·£»
¢ŻÄÜŹ¹pHŹŌÖ½±äĪŖĄ¶É«µÄČÜŅŗÖŠ“ęŌŚ“óĮæĒāŃõøłĄė×Ó£¬Na+”¢C1-”¢S2-”¢SO32- Ö®¼ä²»·“Ó¦£¬¶¼²»ÓėĒāŃõøłĄė×Ó·“Ó¦£¬ŌŚČÜŅŗÖŠÄܹ»“óĮæ¹²“ę£¬¹Ź¢ŻÕżČ·£»
¢ŽĖįŠŌČÜŅŗÖŠ£ŗFe2+”¢I-ŗĶNO3-·¢ÉśŃõ»Æ»¹Ō·“Ó¦¶ų²»ÄÜ“óĮæ¹²“ę£¬¹Ź¢Ž“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó¹²“ę£¬ĪŖøßĘµæ¼µć£¬ĢāÄæÄѶČÖŠµČ£¬²ąÖŲæ¼²éø“·Ö½ā·“Ó¦”¢Ńõ»Æ»¹Ō·“Ó¦£¬Ć÷Č·Ąė×ÓŠŌÖŹ¼°Ąė×Ó¹²“ęĢõ¼žŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢ŅāŅžŗ¬Ģõ¼žµÄĶŚ¾ņ£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
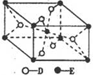 ŅŃÖŖA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪµŻŌö£¬A”¢B”¢C”¢DĪ»ÓŚ¶ĢÖÜĘŚ£®AŹĒŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£»BµÄ»łĢ¬Ō×ÓÖŠµē×ÓÕ¼¾ŻČżÖÖÄÜĮæ²»Ķ¬µÄŌ×Ó¹ģµĄ£¬ĒŅĆæÖÖ¹ģµĄÖŠµÄµē×Ó×ÜŹżĻąĶ¬£»DŌ×ÓµÄŗĖĶā³É¶Ōµē×ÓŹżŹĒĪ“³É¶Ōµē×ÓŹżµÄ3±¶£»EÓŠ”°ÉśĪļ½šŹō”±Ö®³Ę£¬E4+ŗĶė²Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼ĻąĶ¬£®A”¢B”¢DČżÖÖŌŖĖŲ×é³ÉµÄŅ»ÖÖ»ÆŗĻĪļMŹĒŠĀ×°ŠŽ¾ÓŹŅÖŠ³£ŗ¬ÓŠµÄŅ»ÖÖÓŠŗ¦ĘųĢ壬A”¢BĮ½ÖÖŌŖĖŲ×é³ÉµÄŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ1µÄ»ÆŗĻĪļNŹĒ³£¼ūµÄÓŠ»śČܼĮ£®
ŅŃÖŖA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪµŻŌö£¬A”¢B”¢C”¢DĪ»ÓŚ¶ĢÖÜĘŚ£®AŹĒŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£»BµÄ»łĢ¬Ō×ÓÖŠµē×ÓÕ¼¾ŻČżÖÖÄÜĮæ²»Ķ¬µÄŌ×Ó¹ģµĄ£¬ĒŅĆæÖÖ¹ģµĄÖŠµÄµē×Ó×ÜŹżĻąĶ¬£»DŌ×ÓµÄŗĖĶā³É¶Ōµē×ÓŹżŹĒĪ“³É¶Ōµē×ÓŹżµÄ3±¶£»EÓŠ”°ÉśĪļ½šŹō”±Ö®³Ę£¬E4+ŗĶė²Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼ĻąĶ¬£®A”¢B”¢DČżÖÖŌŖĖŲ×é³ÉµÄŅ»ÖÖ»ÆŗĻĪļMŹĒŠĀ×°ŠŽ¾ÓŹŅÖŠ³£ŗ¬ÓŠµÄŅ»ÖÖÓŠŗ¦ĘųĢ壬A”¢BĮ½ÖÖŌŖĖŲ×é³ÉµÄŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ1µÄ»ÆŗĻĪļNŹĒ³£¼ūµÄÓŠ»śČܼĮ£®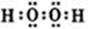 £¬EµÄ»łĢ¬Ō×ÓµÄĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ3d24s2£®
£¬EµÄ»łĢ¬Ō×ÓµÄĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ3d24s2£®| t/”ę | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«40g NaOHČܽāŌŚ1LĖ®ÖŠ | |
| B£® | ½«25g µØ·ÆČÜÓŚĖ®Åä³É100mL CuSO4ČÜŅŗ | |
| C£® | ½«0.1L 10 mol•L-1ÅØĮņĖį¼ÓČė0.9LĖ®ÖŠ | |
| D£® | ½«22.4L HClĘųĢåČÜÓŚĖ®Åä³É1LČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeSO4”¢Fe£ØNO3£©3£» Fe2£ØSO4£©3”¢HNO3”¢N2O”¢H2O | |
| B£® | HNO3”¢FeSO4£» Fe2£ØSO4£©3”¢Fe£ØNO3£©3”¢N2O”¢H2O | |
| C£® | HNO3”¢Fe2£ØSO4£©3£» FeSO4”¢Fe£ØNO3£©3”¢N2O”¢H2O | |
| D£® | Fe2£ØSO4£©3”¢N2O£» FeSO4”¢HNO3”¢Fe£ØNO3£©3”¢H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ijæĪĶā»ī¶ÆŠ”×éÓĆČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
ijæĪĶā»ī¶ÆŠ”×éÓĆČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ć÷·Æ¾»Ė® | B£® | ¹¤Ņµ¹ĢµŖ | C£® | ŗ£Ė®ĢįĆ¾ | D£® | µē³Ų³äµē |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃé¢ŁÖŠ²śÉśµÄĘųĢåĪŖ°±Ęų£¬²¢æɵĆŌČÜŅŗÖŠc£ØNH4+£©=0.2 mol•L-1 | |
| B£® | ŹµŃé¢ŪÖŠµÄ°×É«³ĮµķÖŠŅ»¶ØÓŠBaSO4£¬ĪŽBaCO3 | |
| C£® | ŌČÜŅŗÖŠŅ»¶ØÓŠK+£¬ĒŅc£ØK+£©=0.4 mol•L-1 | |
| D£® | ČōŅŖÅŠ¶ĻŌČÜŅŗÖŠŹĒ·ńÓŠCl-£¬ĪŽŠčĮķĶāÉč¼ĘŹµŃéŃéÖ¤ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{3}{£Øm-n£©}$mL | B£® | $\frac{£Øm-n£©}{3}$ mL | C£® | $\frac{£Ø4m-1£©}{13}$ mL | D£® | $\frac{£Øm-n£©}{3}$3 mL |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com