
 £Ø2010?ĻęĢ¶ČżÄ££©”°ÉńĘß”±µĒĢģ±źÖ¾×ÅĪŅ¹śµÄŗ½ĢģŹĀŅµ½ųČėĮĖŠĀµÄĘŖÕĀ£®ĒėÄć½ā“šÓŠ¹ŲĪŹĢā£ŗ
£Ø2010?ĻęĢ¶ČżÄ££©”°ÉńĘß”±µĒĢģ±źÖ¾×ÅĪŅ¹śµÄŗ½ĢģŹĀŅµ½ųČėĮĖŠĀµÄĘŖÕĀ£®ĒėÄć½ā“šÓŠ¹ŲĪŹĢā£ŗ

 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø2010?ĻęĢ¶ČżÄ££©Ä³×°ÖĆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø””””£©
£Ø2010?ĻęĢ¶ČżÄ££©Ä³×°ÖĆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
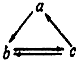 £Ø2010?ĻęĢ¶ČżÄ££©ĻĀ±ķĖłĮŠø÷ĪļÖŹ×éÖŠ£¬ĪļÖŹa”¢b”¢cÖ®¼äĶعżŅ»²½·“Ó¦¾ĶÄÜŹµĻÖČēĶ¼ĖłŹ¾×Ŗ»ÆµÄŹĒ£Ø””””£© £Ø2010?ĻęĢ¶ČżÄ££©ĻĀ±ķĖłĮŠø÷ĪļÖŹ×éÖŠ£¬ĪļÖŹa”¢b”¢cÖ®¼äĶعżŅ»²½·“Ó¦¾ĶÄÜŹµĻÖČēĶ¼ĖłŹ¾×Ŗ»ÆµÄŹĒ£Ø””””£©
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø2010?ĻęĢ¶ČżÄ££©N2O5ŹĒŅ»ÖÖŠĀŠĶĻõ»Æ¼Į£¬Ä³ĪĀ¶ČĻĀÓŠ·“Ó¦£ŗ2N2O5£Øg£©?4NO2£Øg£©+O2£Øg£©£¬”÷H£¾0£¬ĻĀ±ķĪŖT1ĪĀ¶ČĻĀµÄ²æ·ÖŹµŃ鏿¾Ż£ŗ
|
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com