
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志。目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2 2SO3,的说法不正确的是( )
2SO3,的说法不正确的是( )
A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年江西省高二上第二次月考化学试卷(解析版) 题型:选择题
下列描述中正确的是
A.强酸与强碱反应都是放热反应
B.氧化还原反应一定都是放热反应
C.放热反应的反应速率总是大于吸热反应的反应速率
D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的 不同
不同
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期第二次检测化学试卷(解析版) 题型:填空题
Cl2是重要的化工原料。
(1)写出用Cl2制备漂白液的离子方程式______________________。

(2)图1所示的催化剂循环可实验用O2将HCl转化为Cl2,其中反应①为2HCl(g)+CuO(s) H2O(g)+CuCl2(s) ΔH1,反应②消耗1mol O2的反应热为△H2,则总反应生成1mol Cl2(g)的焓变为 (用ΔH1和ΔH2表示)。
H2O(g)+CuCl2(s) ΔH1,反应②消耗1mol O2的反应热为△H2,则总反应生成1mol Cl2(g)的焓变为 (用ΔH1和ΔH2表示)。
(3)实验室模拟用O2将HCl转化为Cl2的总反应
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的ɑHCl—T曲线如图2所示,则总反应的△H_________0 ,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是 ,简要说明理由: 。
②在上述实验中若压缩体积使压强增大,在图2中画出相应ɑHCl—T曲线的示意图。
③为提高HCl的平衡转化率下列措施中可行的是 。
A.增大n(HCl) B.增大n(O2) C.使用更好的催化剂 D.移去H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二12月月考化学试卷(解析版) 题型:选择题
在Na2S溶液中c(Na+)与c(S2-)的比值是
A.2 B.小于2 C.大于2 D.1/2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州遵义航天中学高二上第三次月考化学卷(解析版) 题型:?????
对于可逆反应2AB3(g) 2A(g) + 3B2(g) △H>0,下列图像不正确的是( )
2A(g) + 3B2(g) △H>0,下列图像不正确的是( )
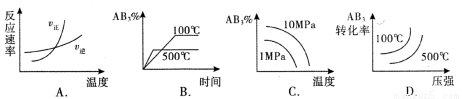
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州遵义航天中学高二上第三次月考化学卷(解析版) 题型:?????
反应的离子方程式中,正确的是 ( )
A.铁与稀硫酸反应 Fe+2H+=Fe3++H2↑
B.氢氧化铝与足量盐酸反应 Al(OH)3+3H+=Al3++3H2O
C.钠和冷水反应 Na+2H2O=Na++H2↑+OH-
D.金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州遵义航天中学高一上第三次月考化学卷(解析版) 题型:选择题
下列实验设计方案中,可行的是( )
A.用加入过量铁粉的方法除去Cu(NO3) 2溶液中混有的AgNO3
B.用NaOH溶液除去CO2中混有的HCl气体
C.向某无色未知溶液中加入BaCl2溶液,以检验未知溶液中是否含有SO42-
D.用紫色石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中必修化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.碳酸钙溶于醋酸 CaCO3+ 2H+ = Ca2+ + CO2↑ + H2O
B.氢氧化钠溶液吸收二氧化硫气体 SO2 + 2OHˉ= SO42ˉ+ H2O
C.氯气溶于水 Cl2+H2O===2H+ + Cl-+ClO-
D.氯化铁溶液溶解铜 Cu + 2Fe3+ =Cu2+ + 2Fe2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高一上期中测试化学试卷(解析版) 题型:填空题
实验室用氯酸钾和二氧化锰制取氧气的反应方程式为:
2KClO3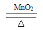 2KCl+3O2↑
2KCl+3O2↑
回答下列问题:
(1)该反应中被氧化的元素名称为_________,还原产物的化学式是________,生成1molO2时转移电子的数目是____________。
(2)从反应后的固体混合物中分离出难溶于水的MnO2具体操作步骤:____________。
(3)分离出的MnO2可用于实验室制取Cl2,化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,其离子方程式为____________。
MnCl2+Cl2↑+2H2O,其离子方程式为____________。
(4)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为_______。
(5)以上两个反应都用到MnO2,其作用分别是________、________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com