
【题目】根据下面各物质之间的转化关系,回答问题:
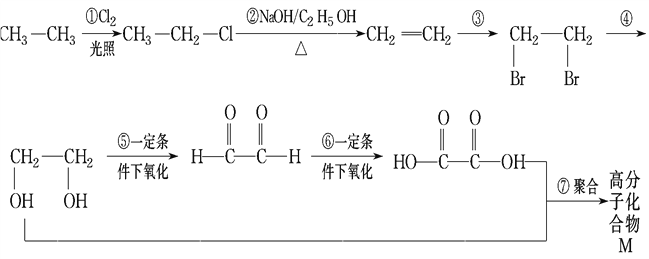
(1)属于取代反应的是___________。
(2)属于加成反应的是___________。
(3)写出反应③、④的化学方程式(有机物用结构简式表示,注明反应条件,下同)
a.反应③___________________________________________________________。
b.反应④__________________________________________________________。
c.写出![]() 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式 ____________。
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式 ____________。
【答案】 ①④ ③ CH2=CH2 + Br2 ―→CH2BrCH2Br CH2BrCH2Br + 2NaOH![]() 2NaBr + CH2(OH)CH2OH OHCCHO +NaOH+2 Cu(OH)2
2NaBr + CH2(OH)CH2OH OHCCHO +NaOH+2 Cu(OH)2![]() OHCCOONa +Cu2O+3H2O或者 OHCCHO +2 NaOH+4Cu(OH)2
OHCCOONa +Cu2O+3H2O或者 OHCCHO +2 NaOH+4Cu(OH)2![]() NaOOCCOONa +2Cu2O+6H2O
NaOOCCOONa +2Cu2O+6H2O
【解析】试题分析:本题以有机物之间的转化为载体,考查有机反应类型的判断,有机方程式的书写。反应①为CH3CH3与Cl2光照下发生取代反应生成CH3CH2Cl,反应②为CH3CH2Cl在NaOH/C2H5OH、加热条件下发生消去反应生成CH2=CH2,反应③为CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,反应④为CH2BrCH2Br在NaOH水溶液、加热条件下发生取代反应生成HOCH2CH2OH,反应⑤为HOCH2CH2OH发生氧化反应生成OHCCHO,反应⑥为OHCCHO发生氧化反应生成HOOCCOOH,反应⑦为HOCH2CH2OH与HOOCCOOH发生缩聚反应生成高分子化合物![]() 。
。
(1)根据上述分析,属于取代反应的是①④。
(2)根据上述分析,属于加成反应的是③。
(3)a.反应③的化学方程式为CH2=CH2+Br2→CH2BrCH2Br。
b.反应④的化学方程式为CH2BrCH2Br + 2NaOH![]() 2NaBr + CH2(OH)CH2OH。
2NaBr + CH2(OH)CH2OH。
c.OHCCHO中含2个醛基,所以与新制Cu(OH)2悬浊液反应时物质的量之比不同产物不同,反应的化学方程式为OHCCHO +NaOH+2 Cu(OH)2![]() OHCCOONa +Cu2O+3H2O或者 OHCCHO +2 NaOH+4Cu(OH)2
OHCCOONa +Cu2O+3H2O或者 OHCCHO +2 NaOH+4Cu(OH)2![]() NaOOCCOONa +2Cu2O+6H2O。
NaOOCCOONa +2Cu2O+6H2O。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】环境污染已严重危害人类的生活。下列对应关系正确的是( )
选项 | 环境问题 | 造成环境问题的主要物质 |
A | 温室效应 | CO2 |
B | 南极臭氧层空洞 | SO2 |
C | 酸雨 | O3 |
D | 光化学烟雾 | N2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类对能源的需求不断增加,开发新能源成为当前国际能源研究的重要课题。下列能量转化过程,不涉及化学变化的是
A.利用太阳能分解水制备氢气B.利用氢氧燃料电池提供电能
C.利用风驱动风轮机发电D.利用植物秸秆为原料生产沼气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“碳呼吸电池”是一种新型能源装置,其工作原理如图所示。下列有关说法中错误的是

A. 该装置将化学能转变为电能
B. 利用该技术可捕捉大气中的CO2
C. 该装置工作时,正极上的电极反应式为2CO2-2e-=C2O42-
D. 该装置工作时,理论上每生成1 mol 草酸铝,电路中通过6 mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氯及其化合物的说法不正确的是
A. 氯气能溶于水,常温常压下,1体积水约能溶解2体积氯气
B. 液氯是纯净物,而氯水是混合物,氯气、液氯是同一种物质,只是状态不同
C. 氯气可用于自来水的消毒、农药的生产、药物的合成
D. 氯气通入水中能置换出氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某2.0L硫酸溶液中含有1.0mol H2SO4 . 向上述溶液中加入足量铁粉,试回答下列问题:
(1)写出该反应的离子方程式;
(2)溶液中H2SO4的物质的量浓度;
(3)产生气体的体积(标准状况);
(4)假设反应前后溶液体积不变,则所得溶液中Fe2+的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中,发生以下反应:2A(g)+ B(g) ![]() 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
A. 1.6 mol B. 2.8 mol C. 2.4 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,体积不变的密闭容器中发生如下反应:A(g) ![]() 2B(g) ΔH>0,每隔一定时间对该容器内的物质进行分析,得到如下表格,试填空:
2B(g) ΔH>0,每隔一定时间对该容器内的物质进行分析,得到如下表格,试填空:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(A)(mol/L) | 0.100 | c1 | 0.050 | c3 | c4 | c5 |
c(B) (mol/L) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)达到平衡时A的转化率为________。在此条件下,平衡常数K为______。
(2)在0~60s时间段内,A的平均反应速率为_________________。
(3)要使平衡向正反应方向移动,可采取的措施______(填序号)。
A、体积不变时增大的A起始浓度 B、升高温度
C、使用催化剂 D、缩小容器体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com