
下列过程中颜色变化与化学变化无关的是( )
A.银白色的金属铁研磨成铁粉后变成黑色
B.新切割开的金属钠的表面由银白色迅速变成暗灰色
C.红棕色的NO2通过装有水的洗气瓶后得到无色气体
D.浅黄绿色的新制氯水久置后变为无色
科目:高中化学 来源:2016-2017学年福建省高一上第一次月考化学卷(解析版) 题型:选择题
有15g Na2O2、Na2O、NaOH的混合物与400 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为
A.23.4 g B.25.5g C.31 g D.无法计算
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上第一次月考化学卷(解析版) 题型:选择题
某学生欲完成2HCl+2Ag═2AgCl+H2↑反应,设计了下列四个实验,你认为可行的实验是
A. B. C. D.
查看答案和解析>>
科目:高中化学 来源:2017届山东省新泰市高三上学期第一次阶段考化学试卷(解析版) 题型:选择题
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是
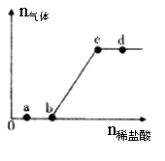
A.a点对应的溶液中:Na+、OH-、SO42-、NO3-
B.b点对应的溶液中:Al3+、Fe3+、MnO4-、Cl-
C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源:2017届山东省新泰市高三上学期第一次阶段考化学试卷(解析版) 题型:选择题
分类法是学习化学的重要方法,人们在认识事物时可采用多种分类方法。下表(2)中的物质不能与(1)中的物质归为一类的是( )
选项 | (1) | (2) |
A | FeSO4、NO2、MnO2、NaClO、Na2O2 | H2SO3 |
B | CH3COOH、HOOC—COOH、HClO、H2S | HF |
C | 复分解反应、电极反应、放热反应、离子反应 | 焰色反应 |
D | (NH4)2SO4、NH4Cl、NH4NO3、NH3·H2O | NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源:2017届山东省高密市高三上学期10月统考化学试卷(解析版) 题型:填空题
研究发现,含pm2.5的雾霾主要成分有SO2、NOx、CxHy及可吸入颗粒等。
(1)雾霾中能形成酸雨的物质是_____________。
(2)为消除NOx对环境的污染,可利用NH3在一定条件下与NO反应生成无污染的气体。
已知:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H = -905.48 kJ·mol-1
4NO(g)+6H2O(g) △H = -905.48 kJ·mol-1
N2(g)+O2(g) 2NO(g) △H = +180.50 kJ·mol-1
2NO(g) △H = +180.50 kJ·mol-1
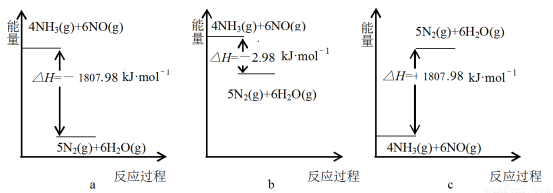
①下列表示NH3(g)与NO(g)在一定条件下反应,生成无污染气体的能量转化关系示意图正确的是:___________(填字母)
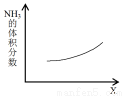
② 右图是反应4NH3(g)+6NO(g) 5N2(g)+6H2O(g)过程中NH3的体积分数随X变化的示意图,X代表的物理量可能是_________,原因是_________。
5N2(g)+6H2O(g)过程中NH3的体积分数随X变化的示意图,X代表的物理量可能是_________,原因是_________。
(3)如图电解装置可将雾霾中的SO2、NO转化为(NH4)2SO4,
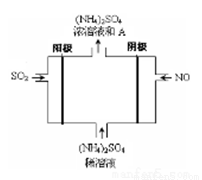
① 阴极的电极反应式是 。
② 物质A是_____________(填化学式),理由是_________________________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省高密市高三上学期10月统考化学试卷(解析版) 题型:选择题
探究铜与浓硝酸的反应,下列装置或操作正确的为

A. 用装置①进行铜和浓硫酸的反应 B. 用装置②收集二氧化硫并吸收尾气
C. 用装置③稀释反应后的混合液 D. 用装置④测定余酸的浓度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:填空题
侯氏制碱法曾广泛用于工业制纯碱(Na2CO3),是我国科学家为人类做出的重大贡献.现有25℃时,浓度为0.10mol/LNa2CO3溶液.请回答:
(1)该溶液中c(H+) c(OH﹣) (填“>”、“=”或“<”).
(2)用离子方程式解释(1)的原因: .
(3)下列说法正确的是(填字母) .
a.Na2CO3在水中完全电离
b.c(CO32﹣)+c(HCO3﹣)+c(H2CO3)=0.1mol/L
c.c(Na+)>c(CO32﹣)>c(OH﹣)>c(HCO3﹣)>c(H+)
(4)用石墨作电极电解Na2CO3水溶液时,阴极反应式是 .
(5)Na2CO3溶液中的电荷守恒关系式为:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东实验中学顺德学校高二上阶段质检化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
B.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
D.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com