
【题目】蛋白质是人体必需的重要营养成分之一。下列食物中,富含蛋白质的是
A.豆腐B.馒头C.西红柿D.豆油
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有机物A的结构简式如图所示:下列有关A的性质叙述中,错误的是
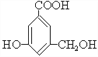
A. 与金属钠完全反应时,两者物质的量之比为1:3
B. 与氢氧化钠完全反应时,两者物质的量之比为1:1
C. 与碳酸氢钠溶液反应时,两者物质的量之比为1:2
D. 在一定条件下,既能与羧酸反应,又能与醇反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 第ⅠA 族元素的金属性比第ⅡA 族元素的金属性强
B. 第ⅦA 族元素单质的熔点从上到下逐渐升高
C. 第ⅥA 族元素的氢化物中,稳定性最好的元素非金属性最弱
D. 第三周期元素的离子半径从左到右逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来AIST报告正在研制一种“高容量、低成本”的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH一,下列说法不正确的是 ( )
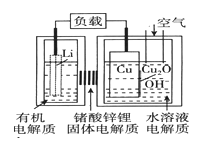
A. 放电时,Li+透过固体电解质向Cu极移
B. 放电时,正极的电极反应式为O2+2H2O+4e一=4OH—
C. 通空气时,铜被腐蚀,表面产生Cu2O
D. 通空气时,整个反应过程中,铜相当于是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4 制备路线如下:
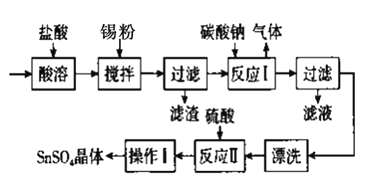
查阅资料:
I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡[Sn(OH)C1]。
回答下列问题:
(1)操作I的步骤为_____________________、过滤、洗涤、干燥。过滤后滤液仍混浊的原因是(除滤纸破损,所有仪器均洗涤干净)__________________________、__________________________.
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式及化学反应原理解释原因:
_________________________________________________
(3)加入锡粉的作用有两个:①调节溶液pH;②_____________________。
(4)SnS04还可在酸性条件下用作双氧水的去除剂,发生反应的离子方程式是______________________________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取质量为m g的锡粉溶于稀硫酸中,向生成的SnSO4中加入过量的Fe2(SO4)3溶液,用物质的量浓度为c mol/L的K2Cr207标准溶液滴定生成的Fe2+,共用去K2Cr207溶液的体积为V L。 则锡粉中锡的质量分数是_______________。(Sn的摩尔质量为M g/mol,用含m、c、V、M的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍在金属羰基化合物(金属元素和CO中性分子形成的一类配合物)、金属储氢材料(能可逆地多次吸收、储存和释放H2的合金)等领域用途广泛。
(1)基态Ni原子核外电子排布式为__________________________。
(2)Ni(CO)4中镍元素的化合价为__________,写出与CO互为等电子体的带一个单位正电荷的阳离子为:_______。Ni(CO)4的一氯代物有2种,其空间构型为_______________ o
(3)一种储氢合金由镍与镧(La)组成,其晶胞结构如图所示,则该晶体的化学式为_____________

(4)下列反应常用来检验Ni2+,请写出另一产物的化学式:_______________。
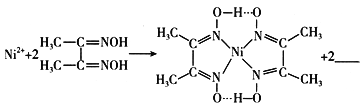
与Ni2+配位的N原子有__________个,该配合物中存在的化学键有_________(填序号)。
A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(5)Ni与Fe的构型相同(体心立方堆积),Ni的摩尔质量为M g/mol,阿伏加德罗常数为NA,密度为a g/cm3Ni原子的半径为_________pm(金属小球刚性相切)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氨气易溶于水生成氨水,氨水电离生成铵根离子,铵根离子中氮原子采取________杂化,NH4+中HNH键角比NH3中HNH键角大,原因是__________________。
(2)Cu3N形成的晶体结构如图所示,N3-的配位数是________________。

(3)常温常压下,给水施加一个弱电场便可形成冰,称之为“热冰”,热冰中微粒间存在的作用力有________,其大小顺序是__________。
(4)NaF和NaCl属于同一主族的钠盐,但NaF的莫氏硬度比NaCl大,原因是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com