

 ����M��һ�ֺϳ�·����ͼ�����ַ�Ӧ�Լ�������ʡ�ԣ���
����M��һ�ֺϳ�·����ͼ�����ַ�Ӧ�Լ�������ʡ�ԣ���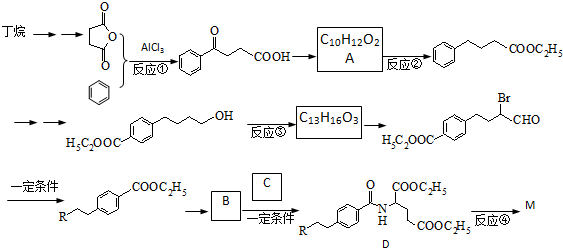
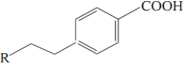 ��C
��C ��
�� ��
��
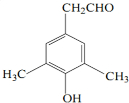
���� �����̿�֪�����龭���������ɶ����������Ȼ�������������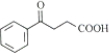 ���Ա�
���Ա� �ͷ�Ӧ�ڵIJ����֪AӦΪ
�ͷ�Ӧ�ڵIJ����֪AӦΪ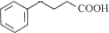 ��
��
�Աȷ�Ӧ�����֪����ʽΪC13H16O3�����ʵĽṹ��ʽΪ ��B��C����ȡ����Ӧ�����ļ����ɷ�Ӧ���̿�֪BӦΪ
��B��C����ȡ����Ӧ�����ļ����ɷ�Ӧ���̿�֪BӦΪ ��CΪ
��CΪ ������л���Ľṹ�������Լ���ĿҪ������⣮
������л���Ľṹ�������Լ���ĿҪ������⣮
��� �⣺�����̿�֪�����龭���������ɶ����������Ȼ������������� ���Ա�
���Ա� �ͷ�Ӧ�ڵIJ����֪AӦΪ
�ͷ�Ӧ�ڵIJ����֪AӦΪ ��
��
�Աȷ�Ӧ�����֪����ʽΪC13H16O3�����ʵĽṹ��ʽΪ ��B��C����ȡ����Ӧ�����ļ����ɷ�Ӧ���̿�֪BӦΪ
��B��C����ȡ����Ӧ�����ļ����ɷ�Ӧ���̿�֪BӦΪ ��CΪ
��CΪ ��
��
��1�����龭���������ɶ����������Ȼ������������� ��Ϊȡ����Ӧ����Ӧ�۵ı仯Ϊ�ǻ�����ȩ����Ϊ������Ӧ��
��Ϊȡ����Ӧ����Ӧ�۵ı仯Ϊ�ǻ�����ȩ����Ϊ������Ӧ��
�ʴ�Ϊ��ȡ����Ӧ��������Ӧ��
��2����Ӧ��Ϊ������Ӧ����Ũ�������������Ҵ����ȷ�Ӧ�����ɣ���Ӧ��Ϊ����ˮ�ⷴӦ��Ӧ�����������¼��ȷ�Ӧ���ɣ�
�ʴ�Ϊ��C2H5OH/Ũ����/���ȣ� ����/���ȣ�
��3�������Ϸ�����֪��BӦΪ ��CΪ
��CΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��4��AΪ ��������FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ������ܷ���������Ӧ��˵������ȩ�����۷�������5�ֲ�ͬ��ѧ��������ԭ�ӣ�
��������FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ������ܷ���������Ӧ��˵������ȩ�����۷�������5�ֲ�ͬ��ѧ��������ԭ�ӣ�
����ܶ�Ӧ��ͬ���칹��Ľṹ��ʽΪ ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
��
��5����2-�ȶ���ϳ�1��3-����ϩ��Ӧ�����������Ƶ��Ҵ���Һ�м��ȷ�����ȥ��Ӧ����2-��ϩ��Ȼ�����ӳɷ�Ӧ����2��3-���嶡�飬����������ȥ��Ӧ����1��3-����ϩ����Ӧ������ΪCH3CHClCH2CH3$��_{��}^{NaOH/C_{2}H_{5}OH}$CH3CH=CHCH3$\stackrel{Br_{2}/CCl_{4}}{��}$CH3CHBrCHBrCH3$��_{��}^{NaOH/C_{2}H_{5}OH}$CH2=CHCH=CH2��
�ʴ�Ϊ��CH3CHClCH2CH3$��_{��}^{NaOH/C_{2}H_{5}OH}$CH3CH=CHCH3$\stackrel{Br_{2}/CCl_{4}}{��}$CH3CHBrCHBrCH3$��_{��}^{NaOH/C_{2}H_{5}OH}$CH2=CHCH=CH2��
���� ������Ҫ�����л���ĺϳɣ�������ѧ���ķ��������Ŀ��飬ע����������Ϣ��Ϊ������Ĺؼ����ѶȲ���ע������л���Ľṹ�����ʣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ�����㵹����ͭ��Һ�����һ���ӿ����ƹܵ��ĸ�ʴ | |
| B�� | þ��ϡ���ᷴӦ���ң���������ƾ�����Լ�����Ӧ���� | |
| C�� | ��ⱥ��ʳ��ˮ������ʱ���������� | |
| D�� | ��ⷨ������ͭ���ô�ͭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | Ħ������Ϊ313.5 g | B�� | ���ڷ����� | ||
| C�� | ����ʽΪC12H19Cl3N2O | D�� | ���ܷ����ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2S?2H++S2- | B�� | KHSO4�TK++HSO4- | ||
| C�� | CH3COOH?H++CH3COO- | D�� | NaH2PO4?Na++H2PO4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������������������ֱ�����������ȫȼ�գ����߷ų��������� | |
| B�� | 1molH2��������������ȫȼ�����ų�����������H2��ȼ���� | |
| C�� | HCl��NaOH��Ӧ���к��ȡ�=-57.3kJ•mol-1����H2SO4��Ca��OH��2��Ӧ���к��ȡ�H=-2����-57.3��kJ•mol-1 | |
| D�� | һ�������£�0.2molSO2��g����0.1molO2��g����ϳ�ַ�Ӧʱ�ų�������Ϊ18kJ������SO2��g��+O2��g���T2SO3��g����H=-180kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ��Һ�п϶�����Fe2+��NO3-��SiO32-��I- | |
| B�� | ԭ��Һ�п϶�����K+��Fe3+��Fe2+��NO3-��SO42- | |
| C�� | ���������ɫ������NO���壬��CO2������� | |
| D�� | Ϊȷ���Ƿ���Cl-����ȡԭ��Һ���������������Һ���۲��Ƿ������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1��NaOH��Һ�е�Na+��ĿΪNA | |
| B�� | ��״����NA��SO3�������ԼΪ22.4L | |
| C�� | ͬ��ͬѹ�������ͬ���κ����壬����������ԭ����Ŀһ����� | |
| D�� | ����1 molFe��OH��3�Ľ�����������Fe��OH��3������С��NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaClO��Һ��ͨ������SO2�� 2ClO-+SO2+H2O=2HClO+SO${\;}_{3}^{2-}$ | |
| B�� | ��Fe2��SO4��3��Һ��ͨ��������H2S Fe3++H2S=Fe2++S��+2H+ | |
| C�� | ��FeBr2��ͨ�����Cl2�� 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| D�� | Fe��OH��3��HI�ķ�Ӧ ��Fe��OH��3+3H+=Fe3++3H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com