
(8分)一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,
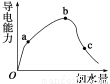
请回答:
(1)O点为什么不导电:_______________________________。
(2)a、b、c三点溶液的pH由小到大的顺序是______________。
(3)H+的物质的量最大的是________(填“a”、“b”或“c”)。
(4)若使c点溶液中的c(CH3COO-)增大,可以采取下列措施中的________(填序号)。
A.加热 B.加很稀的NaOH溶液
C.加NaOH固体 D.加水
E.加入锌粒
18.(8分)(1)无自由移动的离子 (2)b<a<c (3)c (4)ACE
【解析】
试题分析:(1)冰醋酸是纯净的醋酸,只有电解质分子,没有发生电离。没有自由移动的离子所以不能导电。(2)自由移动的离子浓度越大,溶液的导电性就越强,由于导电性b>a>c,所以氢离子的浓度大小顺序是:b>a>c。氢离子的浓度越大,溶液的PH就越小,a,b,c三点的pH由小到大的顺序是b<a<c.(3)加入的水越多,电离的电解质就越多,电离程度就越大。所以 a、b、c三点中电离程度最大的是c,次点H+的物质的量最大;(4)A电解质电离过程是个吸热过程,加热,是温度升高,可以使平衡向电离的方向移动,导致c(CH3COO-)增大,A正确。B.加很稀的NaOH溶液,消耗了氢离子,减小了氢离子的浓度,是电离平衡向电离的方向移动,但由于是稀溶液,最终氢离子的浓度及c(CH3COO-)反而减小,B错误。C.加NaOH固体消耗氢离子,破坏了电离平衡,使电离平衡向电离的方向移动。由于醋酸跟离子没有消耗所以最后c(CH3COO-)增大,C正确。D.加水,平衡正向移动,电解质分子的浓度减小。由于电离平衡移动使c(CH3COO-)增大的趋势小于水对它的稀释作用,最后c(CH3COO-反而减小,D错误。E.加入锌粒消耗氢离子,破坏了电离平衡,促使它向电离的方向移动,最终 c(CH3COO-)增大,E正确。选A C E 。
考点:考查溶液的导电性与溶液稀释的关系及外界条件对电离平衡的影响的知识。


科目:高中化学 来源:2014-2015学年黑龙江哈尔滨第三十二中学高二上学期期中考试化学卷(解析版) 题型:填空题
(4分)判断下列说法是否正确(正确的在括号内打“√”错误的打“×”)
①中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠少于醋酸;( )
②将NaOH和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的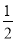 ;( )
;( )
③如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍;( )
④物质的量相同的磷酸钠溶液和磷酸溶液中所含的PO3-4量相同。( )
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期中化学试卷(解析版) 题型:填空题
(9分)取1.43g Na2CO3·XH2O 溶于水配成10mL 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0mL,并收集到112mL CO2(标准状况)。
计算:(1)稀盐酸物质的量浓度为 ;
(2)Na2CO3·xH2O的摩尔质量 ;
(3)x= ;
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期中化学试卷(解析版) 题型:选择题
下列各组微粒中,互为同位素的是
A.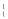 H2 和
H2 和 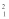 H2 B.
H2 B. Cl 和
Cl 和 Cl
Cl
C.O3 和 O2 D. N 和
N 和 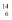 C
C
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期中化学试卷(解析版) 题型:选择题
下列有关分散系说法错误的是
A.胶体区别于其它分散系的本质特征是胶体粒子的直径大小在10-9~10-7m之间
B.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同
D.用肉眼观察,均匀透明的分散系一定是溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学试卷(解析版) 题型:选择题
反应Fe(s)+CO2(g) 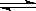 FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是
FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是
A.升高温度该反应的正反应速率增大,逆反应速率减小
B.该反应的化学平衡常数表达式为K=
C.该反应的正反应是吸热反应
D.增大CO2浓度,平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学试卷(解析版) 题型:选择题
把镁条直接投入到盛有盐酸的敞口容器中,产生H2的速率如图所示,
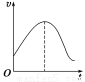
在下列因素中,影响反应速率的因素是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列实验操作或叙述中正确的是
A.蒸发操作时,应使混合物中的水分完全蒸干后再停止加热
B.蒸馏时,温度计水银球需靠近蒸馏烧瓶支管口,冷凝水的流向需从冷凝管的上口进下口流出
C.过滤后洗涤沉淀时,应将固体转移至烧杯中,并加入适量蒸馏水充分搅拌后再过滤
D.分液时,先从分液漏斗下口放出下层液体,更换烧杯后再从上口放出上层液体
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省宁波市高一上学期期中化学试卷(解析版) 题型:选择题
在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一定正确的是
A.加入有色布条,一会儿有色布条褪色。说明溶液中有Cl2存在
B.溶液呈黄绿色,且有刺激性气味,说明有Cl2存在
C.加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明氯水中有Cl-存在
D.加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com