
【题目】由乙烯和其它无机原料合成环状化合物E,请在下列图信回答下列问题:
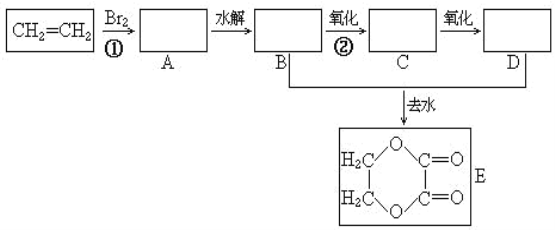
(1)写出①的反应类型______,②所需添加的试剂和反应条件_______
(2)B的结构简式______
(3)E与氢氧化钠溶液反应的化学方程式______。
【答案】加成反应 O2,Cu(或Ag)、加热 HOCH2CH2OH 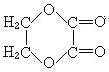 +2NaOH
+2NaOH![]() NaOOC-COONa+HOCH2CH2OH
NaOOC-COONa+HOCH2CH2OH
【解析】
根据流程可知,乙烯发生加成反应生成A :BrCH2-CH2Br;该有机物在碱性环境下发生水解生成B:HOCH2CH2OH;B发生连续氧化,分别生成C:OHC-CHO;D:HOOCCOOH;B与D发生酯化反应生成E: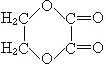 ,据以上分析进行解答。
,据以上分析进行解答。
根据流程可知,乙烯加成反应生成A :BrCH2-CH2Br;该有机物在碱性环境下发生水解生成B:HOCH2CH2OH;B发生连续氧化,分别生成C:OHC-CHO;D:HOOCCOOH;B与D发生酯化反应生成E: ;
;
(1)结合以上分析可知,反应①类型为加成反应;反应②的反应条件为Cu或Ag加热;
故答案是:加成反应;O2,Cu或Ag、加热;
(2)结合以上分析可知,B的结构简式HOCH2CH2OH;
故答案是:HOCH2CH2OH;
(3)E的结构简式: ,在碱性环境下发生水解,反应的化学方程式为:
,在碱性环境下发生水解,反应的化学方程式为: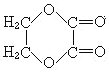 +2NaOH
+2NaOH![]() NaOOC-COONa+HOCH2CH2OH;
NaOOC-COONa+HOCH2CH2OH;
故答案是: +2NaOH
+2NaOH![]() NaOOC-COONa+HOCH2CH2OH。
NaOOC-COONa+HOCH2CH2OH。


科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水溶液中的电离方程式
①H2SO4—____________________;
②Ba(OH)2—____________________;
③NaCl—____________________;
④CuSO4—____________________;
⑤Na2CO3—____________________;
⑥NH4NO3—____________________;
(2)写出下列微粒的结构示意图
①H____________________;
②Na____________________;
③O2-____________________;
④Mg2+____________________;
⑤最外层电子数为次外层电子数2倍的原子____________________;
⑥第二层电子数为第一层、第三层电子数之和的原子:______________________;
⑦氢元素存在着氕氘氚三种原子,它们的原子核内都含有一个质子,中子数分别为0、1、2,请用![]() 表示这三个原子____________________________________,这三种原子的关系是互为_____________。
表示这三个原子____________________________________,这三种原子的关系是互为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5mol·L-1CH3COONa溶液和水的pH随温度的变化如图所示,下列分析错误的是
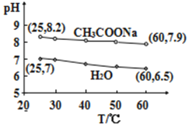
A.25℃,CH3COONa溶液的pH=8.2,显碱性
B.60℃,H2O中c(H+)=1×10-6.5mol·L-1,呈中性
C.60℃,CH3COONa溶液中c(OH-)=1×10-5.1mol·L-1
D.升高温度,CH3COONa溶液水解程度和pH都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(9分)现有含NaCL、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现CL-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
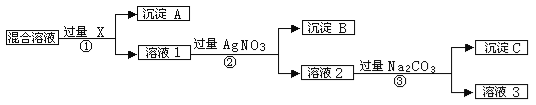
请回答下列问题:
⑴写出实验中下列物质的化学式:试剂X :_______,沉淀A:_______,沉淀B:______。
⑵上述实验流程中加入过量的Na2CO3的目的是___________________________________。
⑶按此实验方案得到的溶液3中肯定含有___________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________ ,之后若要获得固体NaNO3需进行的实验操作是________________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出化学方程式:
(1)丙烯和氯气的取代反应:________。
(2)由苯酚和甲醛合成酚醛树脂:________。
(3)苯酚和浓溴水反应:_________。
(4)烷烃的燃烧通式:_____。
(5)实验室制备乙烯的反应原理:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨碱法(索氏)和联合制碱法(侯氏)对比分析,错误的是
A.产品完全相同B.生产NaHCO3的反应原理相同
C.食盐利用率不同D.都循环利用了CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化镁(MgO2)不溶于水,与酸反应生成H2O2,在医学上可作解酸剂。常温下MgO2较稳定,加热时会分解生成O2和MgO。MgO与H2O2反应可制得MgO2,同时放出大量热。一种制备MgO2的流程如图所示:
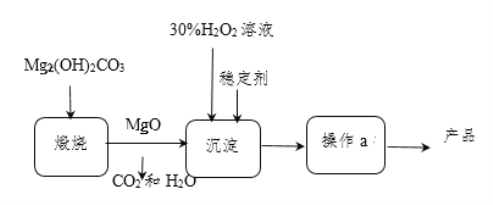
请回答下列问题:
(1)煅烧Mg2(OH)2CO3的化学反应方程式为_______________________;检验Mg2(OH)2CO3已分解完全的方法是______________________________。(写出实验操作和现象)
(2)上述制备过程中加入稳定剂的作用是___________;操作a为_____________。
MgO2产品中常会混有少量MgO,实验室可通过多种方案测定样品中MgO2的含量。某研究小组拟用下图装置测定样品(含MgO杂质)中MgO2的含量。
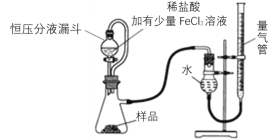
(3)研究小组的实验原理是(用化学方程式表示)①___________________________;
②2H2O2 → 2H2O +O2↑,稀盐酸中加入少量FeCl3溶液的作用是_______________。
(4)实验中使用恒压分液漏斗的优点是:使分液漏斗中的溶液顺利滴下、___________。
(5)反应结束后,先_________________,然后__________________,最后平视刻度线读数并记录。
(6)该小组记录的实验数据如下,样品的质量为m g;反应开始前量气管的读数为a mL;反应结束后量气管的读数为b mL,则样品中过氧化镁的质量分数为______(该实验条件下O2密度为ρ gL-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有氮及其化合物的转化关系如下图,则下列说法错误的是
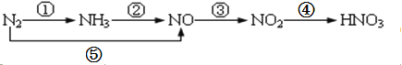
A.路线①②⑤均能表示氮的固定
B.路线②③④是工业生产硝酸的主要途径
C.路线⑤③④是“雷雨发庄稼”的主要途径
D.上述所有反应都是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com