
| 3.16g |
| 158g/mol |
| 3.16g |
| 158g/mol |
| 0.02mol |
| 2 |
| 0.02mol |
| 2 |
| 0.02mol |
| 2 |


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
| A、32 g |
| B、33 g |
| C、32 g?mol-1 |
| D、33 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
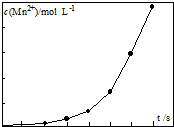 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:
| ||
| K2CO3 | KHCO3 | K2SO4 | KMnO4 | |
| 溶解度/g | 111 | 33.7 | 11.1 | 6.34 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
A Z |
A+1 Z |
| A、质子数相等 | ||
| B、X元素的质量数为A | ||
C、
| ||
| D、它们的化学性质几乎完全相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com