
利用右图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 稀盐酸 | MnO2 | 石蕊溶液 | 石蕊溶液先变红后褪色 | |
B | 浓硫酸 | 蔗糖 | 品红 | 浓硫酸有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | 生成BaSO3白色沉淀 | |
D | 醋酸 | Na2CO3 | 苯酚钠溶液 | 酸性:醋酸>碳酸>苯酚 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:填空题
(物质结构与质性题)X、Y、Z、W是元素周期表前四周期中常见的元素,原子序数依次增大。其相关信息如下表:
元素 | 相关信息 |
X | X的基态原子价层电子中有两个未成对电子 |
Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
Z | Z存在质量数为23,中子数为12的核素 |
W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)X的电负性比Y的________(填“大”或“小”);
X 和Y的气态氢化物中,较稳定的是 (写化学式)。
(2)W在周期表中的位置是 ,其基态原子价电子的电子排布式为 。
(3)Z2Y2的电子式为 ,请写出Z2Y2与XY2反应的化学方程式 。
(4)在XY2分子中X原子的杂化方式为 ,其分子的空间构型为 。氢、X、Y三种元素可共同形成多种分子和一种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一下期中化学试卷(解析版) 题型:选择题
在四个不同容器中,不同条件下进行合成氨反应.根据在相同时间内测定的结果判断生成氨的速率最快的是( )
A.v(N2)=0.1mol•L﹣1•s﹣1 B.v(H2)=0.1mol•L﹣1•min﹣1
C.v(NH3)=0.15mol•L﹣1•min﹣1 D.v(H2)=0.3mol•L﹣1•min﹣1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一下期中化学试卷(解析版) 题型:选择题
下列有关实验的描述不正确的是
A.钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同
B.新制饱和氯水和浓硝酸光照下会有气体产生,其成分中有氧气
C.次氯酸和过氧化钠都能使品红溶液褪色,其原理是不相同的
D.灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO2能与NaOH反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期中化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g)△H1=—99kJ.mol-1,
CH3OH(g)△H1=—99kJ.mol-1,
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H2=—58kJ.mol-1
CH3OH(g)+H2O(g)△H2=—58kJ.mol-1
③CO2(g)+H2(g) CO(g)+H2O(g)△H3
CO(g)+H2O(g)△H3
回答下列问题:
(1)写出CO2的结构式__________。
(2)由上述数据计算出△H3=kJ.mol-1
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,温度T1、T2对反应的影响,下列正确的是__________(填序号)
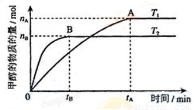
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tAmol/(L·min)
②该反应在T1时的平衡常数比T2时的小
③当生成1mol甲醇的同时,生成1molCO2,说明反应达到平衡
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;该温度条件下,反应平衡常数为__________(计算出结果)
(5)在直接以甲醇为燃料电池中,电解质溶液为硫酸性,负极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期中化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
A.AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
B.CO2通入苯酚钠溶液:2C6H5O-+H2O+CO2→2C6H5OH+CO32-
C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+ 2Fe(OH)3+3Mg2+
2Fe(OH)3+3Mg2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期中化学试卷(解析版) 题型:选择题
能用酸性高锰酸钾溶液鉴别的一组物质是
A.己烷和苯 B.乙烯和乙炔 C.乙醇和乙醛 D.甲苯和苯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古杭锦后旗奋斗中学高一下期中化学卷(解析版) 题型:选择题
如图是部分短周期元素化合价与原子序数的关系图,下列说法中正确的是( )
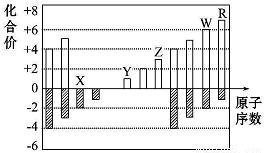
A.Y和Z两者最高价氧化物对应的水化物能相互反应
B.气态氢化物的稳定性:R﹤W
C.WX3和水反应形成的化合物是离子化合物
D.原子半径:Z>Y>X
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽师大附中高二下期中化学试卷(解析版) 题型:填空题
短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的最外层电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为___________________;
(2)已知:①E-E→2E•;△H=+a kJ•mol-1
②2A•→A-A;△H=-b kJ•mol-1
③E•+A•→A-E;△H=-c kJ•mol-1(“•”表示形成共价键所提供的电子)
写出298K时,A2与E2反应的热化学方程式___________________;
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)?X(g);△H=-d J•mol-1(d>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2mol A2、1mol BC | 1mol X | 4mol A2、2mol BC |
平衡时n(X) | 0.5mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 | α1 | α2 | α3 |
①该温度下此反应的平衡常数K的值为_____;
②三个容器中的反应分别达平衡时各组数据关系正确的是_____(填序号)
A.α1+α2=1 B.α3<α1 C.n2<n3<1.0mol D.P3<2P1=2P2 E.Q1+Q2=d F.Q3=2Q1
(4)在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在下图中画出第5min到新平衡时X的物质的量浓度的变化曲线。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com