
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是( )
|
| A. | 两个反应中均为硫元素被氧化 |
|
| B. | 碘元素在反应①中被还原,在反应②中被氧化 |
|
| C. | 氧化性:Mn02>SO42﹣>I03﹣>I2 |
|
| D. | 反应①、②中生成等量的I2时转移电子数比为1:5 |
| 氧化性、还原性强弱的比较;氧化还原反应的电子转移数目计算.. | |
| 专题: | 氧化还原反应专题. |
| 分析: | A.失电子化合价升高的元素被氧化; B.失电子化合价升高的元素被氧化,得电子化合价降低的元素被还原; C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性; D.根据碘和转移电子之间的关系式计算. |
| 解答: | 解:A.在反应①中硫元素既不被氧化也不被还原,在反应②中被氧化,故A错误; B.碘元素在反应①中被氧化,在反应②中被还原,故B错误; C.氧化性I03﹣>SO42﹣,故C错误; D.反应①中生成1mol碘转移2NA电子,反应②中生成1mol碘转移10NA电子,所以反应①、②中生成等量的I2时转移电子数比为2NA:10NA=1:5,故D正确; 故选D. |
| 点评: | 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,注意利用化合价计算转移的电子数,题目难度不大. |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。下列说法不正确的是
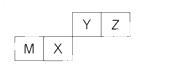
A.原子半径Z<M
B.Y的最离价氧化物对应水化物的酸性比X 的弱
C.X 的最 简单气态氢化物的热稳定性比Z的小
简单气态氢化物的热稳定性比Z的小
D.Z位于元索周期表中第2 周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:
mCeO2 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+ xCO2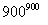 mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
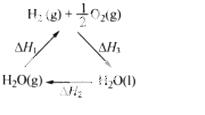 下列说法不正确的是
下列说法不正确的是
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中△H1=△H2+△H3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO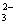 +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是一种可再生能源,具 有广泛的开发和应用前景。
有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g)  CH
CH 3OH(g)+H2O(g) ΔH2
3OH(g)+H2O(g) ΔH2
①上述反应符合“原子经济”原则的是________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250 ℃ | 300 ℃ | 350 ℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断,ΔH1______0(填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为________(从上表中选择)。
H2充入2 L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为________(从上表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566.0  kJ·mol-1
kJ·mol-1
③H2O(g)===H2O(l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
|
| A. | 1.0mol•L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣ |
|
| B. | 含有大量Fe2+的溶液中:H+、Mg2+、ClO﹣、NO3﹣ |
|
| C. | c(H+)=10﹣12mol•L﹣1的溶液:K+、Ba2+、Cl﹣、Br﹣ |
|
| D. | 能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32﹣、HCO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
|
| A. | 加入KSCN溶液一定不变红色 | B. | 溶液中一定含Fe2+ |
|
| C. | 溶液中一定不含Cu2+ | D. | 剩余固体中一定含Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含4mol KNO3和2.5mol H2SO4,向其中加入1.5mol铁,充分反应后产生的NO气体在标准状况下的体积为( )
|
| A. | 36L | B. | 22.4L | C. | 28L | D. | 11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据相关实验得出的结论正确的是
A.利用一束强光照射明矾溶液,产生光亮的“通路”,说明明矾一定发生了水解
B.向盛有Fe(NO3)2溶液的试管中加入0.1 mol·L-1 H2SO4溶液,试管口出现红棕色气体, 说明溶液中NO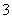 被Fe2+还原为NO2
被Fe2+还原为NO2
C.将某气体通入品红溶液中,品红褪色,说明该气体一定是SO2
D.向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
下列混合溶液中,加入过量的氨水产生沉淀,再加入过量的氢氧化钠溶液,沉淀消失的是( )
A.NaCl和MgCl2 B.NaNO3和KNO3
C.K2SO4和Al2(SO4)3 D.MgCl2和AlCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com