
| A. | 两个反应中均为硫元素被氧化 | |
| B. | 反应①、②中生成等量的I2时转移电子数比为1:5 | |
| C. | 氧化性:MnO2>SO42->IO3->I2 | |
| D. | 碘元素在反应①中被还原,在反应②中被氧化 |
分析 A.失电子化合价升高的元素被氧化;
B.根据碘和转移电子之间的关系式计算;
C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.失电子化合价升高的元素被氧化,得电子化合价降低的元素被还原.
解答 解:A.在反应①中硫元素既不被氧化也不被还原,在反应②中被氧化,故A错误;
B.反应①中生成1mol碘转移2NA电子,反应②中生成1mol碘转移10NA电子,所以反应①、②中生成等量的I2时转移电子数比为2NA:10NA=1:5,故B正确;
C.氧化性I03->SO42-,故C错误;
D.碘元素在反应①中被氧化,在反应②中被还原,故D错误;
故选B.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,注意利用化合价计算转移的电子数,题目难度不大.


科目:高中化学 来源: 题型:选择题
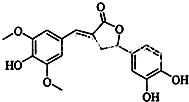
| A. | 分子中含有三种含氧官能团 | |
| B. | 1 mol 该化合物最多能与5mol NaOH反应 | |
| C. | 既可以发生取代反应,又能够发生加成反应 | |
| D. | 能与FeCl3发生显色反应,不能和NaHCO3反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3是氧化剂 | |
| B. | 被氧化与被还原的氯元素的质量比为5:1 | |
| C. | Cl2既是氧化产物又是还原产物 | |
| D. | 0.1mol KClO3 参加反应时有1mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
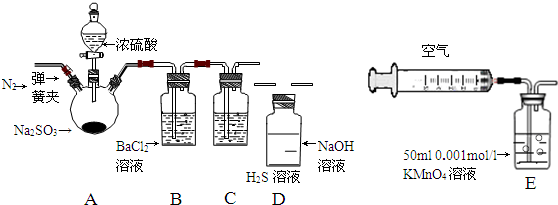
| 实验步骤 | 实验操作 | 预期现象与结论 |
| 1 | 取少量溶液于试管,滴入几滴酚酞 | 溶液变红 |
| 2 | 然后加入足量的BaCl2溶液 | 溶液中产生白色沉淀,最后若红色褪去,则说明①正确;若红色不能褪去,则说明②正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | R |
| W |
| A. | 五种元素的原子最外层电子数一定大于2 | |
| B. | 五种元素一定都是非金属元素 | |
| C. | Z的氧化物与X单质在任何条件下都不会发生置换反应 | |
| D. | R的最外层电子数一定为5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 1 mol甲基的电子数目为10NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
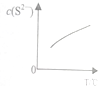 硫粉不溶于水、微溶于酒精,却易溶于Na2S溶液,发生如下反应:(x-1)S(s)+S2-(aq)?Sx2-(aq)(x≤6),达到平衡后,C(S2-)随温度T的变化如图所示.下列有关说法正确的是( )
硫粉不溶于水、微溶于酒精,却易溶于Na2S溶液,发生如下反应:(x-1)S(s)+S2-(aq)?Sx2-(aq)(x≤6),达到平衡后,C(S2-)随温度T的变化如图所示.下列有关说法正确的是( )| A. | 反应(x-1)S(s)+S2-(aq)?Sx2-(aq)的△H>0 | |
| B. | 该反应的平衡常数随温度的升高而减小 | |
| C. | 其他条件不变时,向平衡后的溶液中再加入硫粉,可使溶液中c(Sx2-)增大 | |
| D. | 依此原理,常温下Cl2在饱和NaCl溶液中的溶解度也比在水中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由乙炔制氯乙烯;甲烷与氯气在光照条件下反应 | |
| B. | 溴乙烷和氢氧化钠乙醇溶液共热;乙醇制得乙烯 | |
| C. | 乙烯使溴的四氯化碳溶液褪色;乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 溴乙烷和氢氧化钠溶液共热;乙烯和氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
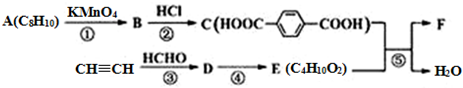
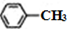 $\stackrel{KMnO_{4}}{→}$
$\stackrel{KMnO_{4}}{→}$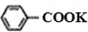
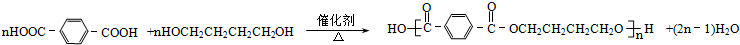 .
.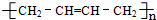
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com