
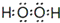 £®
£®·ÖĪö A”¢B”¢C”¢D”¢E”¢F”¢GĘßÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®AŗĶE×īĶā²ćµē×ÓŹżĻąĶ¬£¬¶žÕßĶ¬Ö÷×壬¶ĢÖÜĘŚÖ÷×åŌŖĖŲµÄŌ×ÓÖŠ£¬EŌ×ӵİė¾¶×ī“ó£¬ŌņEĪŖNa£»B”¢CŗĶFŌŚÖÜĘŚ±ķÖŠĻąĮŚ£¬B”¢CĶ¬ÖÜĘŚ£¬C”¢FĶ¬Ö÷×壬ŌņB”¢C“¦ÓŚµŚ¶žÖÜĘŚ£¬F“¦ÓŚµŚČżÖÜĘŚ£¬FŌ×ÓµÄÖŹ×ÓŹżŹĒCŌ×ÓÖŹ×ÓŹżµÄ2±¶£¬ŌņCĪŖOŌŖĖŲ”¢FĪŖSŌŖĖŲ£¬æÉÖŖBĪŖNŌŖĖŲ£»AŗĶCæÉŠĪ³ÉĮ½ÖÖ³£¼ūµÄŅŗĢ¬»ÆŗĻĪļXŗĶY£ØĻą¶Ō·Ö×ÓÖŹĮæX£¼Y £©£¬ŌņAĪŖHŌŖĖŲ£¬XĪŖH2O”¢YĪŖH2O2£»DŠĪ³ÉµÄ·Ö×ÓĪŖµ„Ō×Ó·Ö×Ó£¬ĒŅŌ×ÓŠņŹż½éÓŚŃõ”¢ÄĘÖ®¼ä£¬¹ŹDĪŖNeŌŖĖŲ£»GµÄŌ×ÓŠņŹż“óÓŚĮņ£¬¹ŹGĪŖCl£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA”¢B”¢C”¢D”¢E”¢F”¢GĘßÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®AŗĶE×īĶā²ćµē×ÓŹżĻąĶ¬£¬¶žÕßĶ¬Ö÷×壬¶ĢÖÜĘŚÖ÷×åŌŖĖŲµÄŌ×ÓÖŠ£¬EŌ×ӵİė¾¶×ī“ó£¬ŌņEĪŖNa£»B”¢CŗĶFŌŚÖÜĘŚ±ķÖŠĻąĮŚ£¬B”¢CĶ¬ÖÜĘŚ£¬C”¢FĶ¬Ö÷×壬ŌņB”¢C“¦ÓŚµŚ¶žÖÜĘŚ£¬F“¦ÓŚµŚČżÖÜĘŚ£¬FŌ×ÓµÄÖŹ×ÓŹżŹĒCŌ×ÓÖŹ×ÓŹżµÄ2±¶£¬ŌņCĪŖOŌŖĖŲ”¢FĪŖSŌŖĖŲ£¬æÉÖŖBĪŖNŌŖĖŲ£»AŗĶCæÉŠĪ³ÉĮ½ÖÖ³£¼ūµÄŅŗĢ¬»ÆŗĻĪļXŗĶY£ØĻą¶Ō·Ö×ÓÖŹĮæX£¼Y £©£¬ŌņAĪŖHŌŖĖŲ£¬XĪŖH2O”¢YĪŖH2O2£»DŠĪ³ÉµÄ·Ö×ÓĪŖµ„Ō×Ó·Ö×Ó£¬ĒŅŌ×ÓŠņŹż½éÓŚŃõ”¢ÄĘÖ®¼ä£¬¹ŹDĪŖNeŌŖĖŲ£»GµÄŌ×ÓŠņŹż“óÓŚĮņ£¬¹ŹGĪŖCl£®
£Ø1£©YĪŖH2O2£¬µē×ÓŹ½ĪŖ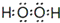 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ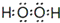 £»
£»
£Ø2£©YĪŖH2O2£¬±»K2Cr2O7Ńõ»ÆĪŖŃõĘų£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒCr2O72-+3H2O2+8H+=2Cr3++3O2+7H2O£¬
¹Ź“š°øĪŖ£ŗCr2O72-+3H2O2+8H+=2Cr3++3O2+7H2O£»
£Ø3£©A”¢C”¢E×é³ÉµÄ»ÆŗĻĪļµÄĖ®ČÜŅŗĪŖNaOHČÜŅŗ£¬½šŹōŅץ¹Žŗ¬ĀĮ£¬Ōņ·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ2Al+2OH-+2H2O=2AlO2-+3H2”ü£¬Éś³ÉµÄĒāĘųŅ×Č¼”¢Ņ×±¬£¬Ōņ“ęŌŚ°²Č«Ņž»¼£¬
¹Ź“š°øĪŖ£ŗ2Al+2OH-+2H2O=2AlO2-+3H2”ü£»ĒāĘųŅ×Č¼”¢Ņ×±¬£»
£Ø4£©PŗĶQĮ½ÖÖĪļÖŹ¶¼ŹĒÓÉH”¢O”¢Na”¢SĖÄÖÖŌŖĖŲ×é³ÉµÄŃĪ£¬ĘäĖ®ČÜŅŗ¶¼ĻŌĖįŠŌ£¬Į½ĪļÖŹĪŖNaHSO3”¢NaHSO4£¬µČĪļÖŹµÄĮæµÄPŗĶQĒ”ŗĆĶźČ«·“Ó¦£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗH++HSO3-ØTSO2”ü+H2O£¬ĮņĖįĒāÄĘŗĶŃĒĮņĖįĒāÄĘÖŠ¾łŗ¬ÓŠĄė×Ó¼üŗĶ¹²¼Ū¼ü£¬
¹Ź“š°øĪŖ£ŗH++HSO3-ØTSO2”ü+H2O£»Ąė×Ó¼üŗĶ¹²¼Ū¼ü£»
£Ø5£©ÓÉA”¢BĮ½ŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļW£¬Ņ»øöW·Ö×ÓŗĶŅ»øöY·Ö×ÓÖŠ¶¼ŗ¬ÓŠ18øöµē×Ó£¬1molŅŗĢ¬WŗĶ2molŅŗĢ¬YĒ”ŗĆĶźČ«·“Ó¦£¬øĆ·“Ó¦·½³ĢŹ½ĪŖ£ŗN2H4+2H2O2=N2+4H2O£¬
¹Ź“š°øĪŖ£ŗN2H4+2H2O2=N2+4H2O£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬×¢Ņā¶ŌŌŖĖŲ»ÆŗĻĪļŠŌÖŹµÄÕĘĪÕ£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £» ¢ŚCl2
£» ¢ŚCl2 £»¢ŪCO2
£»¢ŪCO2 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KCl | B£® | HF | C£® | NaOH | D£® | CaCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| µēĄėÄÜ /£ØkJ•mol-1£© | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | N2ŗĶNH3µÄÖŹĮæ·ÖŹżĻąµČ | |
| B£® | N2”¢H2”¢NH3µÄÅضČÖ®±ČĪŖ1£ŗ3£ŗ2 | |
| C£® | µ±¶ĻæŖ1molµŖµŖČż¼üµÄĶ¬Ź±£¬¶ĻæŖ3molĒāĒā¼ü | |
| D£® | µŖĘųµÄĢå»ż·ÖŹż±£³Ö²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
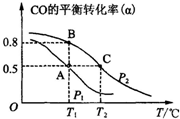 ĄūÓĆCOŗĶH2ŗĻ³É¼×“¼£¬Ęä·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCO£Øg£©+2H2£Øg£©?CH3OH£Øg£©£®½ńŌŚŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ£¬³äÓŠ10mol COŗĶ20mol H2ÓĆÓŚŗĻ³É¼×“¼£®COµÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĪĀ¶Č£ØT£©”¢Ń¹Ēæ£ØP£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
ĄūÓĆCOŗĶH2ŗĻ³É¼×“¼£¬Ęä·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCO£Øg£©+2H2£Øg£©?CH3OH£Øg£©£®½ńŌŚŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ£¬³äÓŠ10mol COŗĶ20mol H2ÓĆÓŚŗĻ³É¼×“¼£®COµÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĪĀ¶Č£ØT£©”¢Ń¹Ēæ£ØP£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČżÖÖŌŖĖŲµÄ×īøßÕż»ÆŗĻ¼ŪÖŠ£¬ZµÄ×ī“ó | |
| B£® | W¾§ĢåÖŠÖ»“ęŌŚÓŠ¹²¼Ū¼ü | |
| C£® | Ō×Ó°ė¾¶£ŗX£¾Y£¾Z | |
| D£® | YµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļŹĒĒæĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ${\;}_{78}^{202}$ PtŗĶ${\;}_{78}^{198}$PtµÄÖŠ×ÓŹżĻąĶ¬£¬»„³ĘĪŖĶ¬Ī»ĖŲ | |
| B£® | ${\;}_{78}^{202}$ PtŗĶ${\;}_{78}^{198}$PtµÄÖŹ×ÓŹżĻąĶ¬£¬»„³ĘĪŖĶ¬Ī»ĖŲ | |
| C£® | ${\;}_{78}^{202}$ PtŗĶ${\;}_{78}^{198}$Pt²»ÄÜ»„³ĘĪŖĶ¬Ī»ĖŲ | |
| D£® | ${\;}_{78}^{202}$PtŗĶ${\;}_{78}^{198}$PtŹĒĶ¬Ņ»ÖÖŗĖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHCO3 | B£® | CH3COOH | C£® | C6H12O6 | D£® | Na2CO3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com