
| A. | 反应体系的总压恒定 | B. | A、B、C、D的物质的量之比为1:3:2:2 | ||
| C. | c(A):c(B)=1:3 | D. | 2V(B)正=3V(C)逆 |
分析 可逆反应A(g)+3B(g)?2C(g)+2D(g)达到平衡状态,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化,注意该反应是气体体积不变的反应,反应过程中压强始终不变.
解答 解:A.由于该反应是气体体积不变的反应,反应过程中气体的总压强始终不变,所以压强不能作为判断平衡状态的标志,故A错误;
B.达到平衡状态时,各物质物质的量之比取决于物质的起始物质的量和反应的转化程度,故不能作为判断是否达到平衡状态的依据,故B错误;
C.c(A):c(B)=1:3,无法判断正逆反应速率是否相等,无法判断是否达到平衡状态,故C错误;
D.2V(B)正=3V(C)逆,表示的是正逆反应速率,且满足二者的化学计量数关系,说明该反应达到了平衡状态,故D正确;
故选D.
点评 本题考查化学平衡状态的判断,题目难度中等,注意化学平衡状态的根本标志是:①v(正) =v(逆),②各组分百分含量不变;在解题时要牢牢抓住这两个根本标志,并明确气体的密度、压强、平均相对分子质量的变化与根本标志的关系.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:填空题
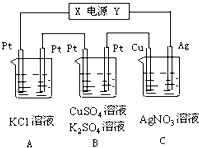 如图所示,若电解5min时铜电极的质量增加2.16g,B中一根Pt电极质量增加0.32g,且此时B中两极都有气体产生.试回答:
如图所示,若电解5min时铜电极的质量增加2.16g,B中一根Pt电极质量增加0.32g,且此时B中两极都有气体产生.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Br的电子式: | |
| B. | S2-的结构示意图: | |
| C. | 氚表示为:${\;}_{1}^{2}$D | |
| D. | 原子核内有l8个中子的氯原子:${\;}_{17}^{36}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.075 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R,金属性L>Q | |
| B. | M与T形成的化合物具有两性 | |
| C. | L2+与R2-的核外电子数相等 | |
| D. | L的原子半径最大,电负性最小,T的原子半径最小,电负性最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体C的物质的量不再改变 | |
| B. | 容器内混合气体的A、B、C的浓度之比为1:3:2 | |
| C. | 单位时间内生成 n mol的A,同时消耗2n mol的C | |
| D. | 正、逆反应均不再进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
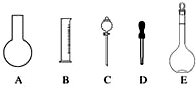 实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
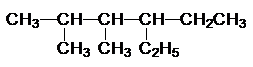 ; TNT:
; TNT: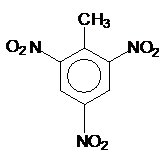 ;
;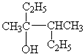 :3,4-二甲基-3-己醇,
:3,4-二甲基-3-己醇,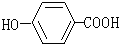 :对羟基苯甲酸.
:对羟基苯甲酸.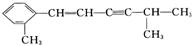 该分子中最多有13个C原子共处同一平面
该分子中最多有13个C原子共处同一平面 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4是酸,因为H2SO4中含有氢元素 | |
| B. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间 | |
| C. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 | |
| D. | Na在Cl2中燃烧不是氧化还原反应,因为没有得氧或失氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入金属钠 | B. | 利用质谱法 | ||
| C. | 利用红外光谱 | D. | 利用核磁共振氢谱仪 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com