
| A. | 可充电的电池称“二次电池”,在充电时,是将电能装化为化学能,在放电时,又将化学能转化为电能 | |
| B. | 在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 | |
| C. | 对于冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法 | |
| D. | 氯化铝的熔点比氧化铝低,因此工业上最好采用电解熔融氯化铝来制备单质铝 |
分析 A.原电池是将化学能转化为电能的装置,电解池是将电能转化为化学能的装置;
B.多数金属中都含有杂质,易形成原电池而发生电化学腐蚀;
C.活泼金属采用电解方法冶炼;
D.工业上采用电解熔融氧化铝的方法冶炼铝.
解答 解:A.原电池是将化学能转化为电能的装置,电解池是将电能转化为化学能的装置,二次电池能多次充放电,所以二次电池在充电时,是将电能装化为化学能,在放电时,又将化学能转化为电能,故A正确;
B.金属与化学物质直接反应而发生化学腐蚀,多数金属中都含有杂质,易形成原电池而发生电化学腐蚀,所以在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大,故B正确;
C.活泼金属采用电解方法冶炼,这几种金属都是活泼金属,所以电解法几乎是唯一可行的工业方法,故C正确;
D.氯化铝是分子晶体,熔融状态下不导电,所以工业上采用电解熔融氧化铝的方法冶炼铝,故D错误;
故选D.
点评 本题考查金属的腐蚀与防护及金属的冶炼,明确原电池原理及金属活泼性与金属冶炼方法的关系即可解答,易错选项是D,注意熔融状态下氯化铝不导电.


科目:高中化学 来源: 题型:选择题
 铅蓄电池是常用的汽车电池.其结构如图所示.铅蓄电池以铅板为负极,表面蒙有大量二氧化铅的铅板作正极,以适当浓度的H2SO4作电解质溶液.已知PbSO4不溶于水也不溶于H2SO4.此电池放电的原理与普通原电池相同,充电时则相当于电解池.下列关于铅蓄电池的说法中正确的是( )
铅蓄电池是常用的汽车电池.其结构如图所示.铅蓄电池以铅板为负极,表面蒙有大量二氧化铅的铅板作正极,以适当浓度的H2SO4作电解质溶液.已知PbSO4不溶于水也不溶于H2SO4.此电池放电的原理与普通原电池相同,充电时则相当于电解池.下列关于铅蓄电池的说法中正确的是( )| A. | 放电时,负极质量减小,正极质量增大 | |
| B. | 放电时,当电路中通过2mol e-时,消耗2mol H2SO4 | |
| C. | 放电时,溶液中SO${\;}_{4}^{2-}$向正极区移动 | |
| D. | 放电时,整个电解质溶液的pH逐渐变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ( Q1+Q2+Q3 ) kJ | B. | 0.5( Q1+Q2+Q3 ) kJ | ||
| C. | ( 0.5Q1-1.5Q2+0.5Q3 ) kJ | D. | ( 3Q1-Q2+Q3 ) kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
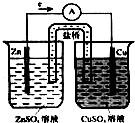 如图是铜锌原电池,又称丹尼尔电池.请回答:
如图是铜锌原电池,又称丹尼尔电池.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径/10-10m | 0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |
 _(R用元素符号表示).
_(R用元素符号表示).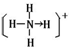 ,含有的化学键类型共价键、配位键.
,含有的化学键类型共价键、配位键.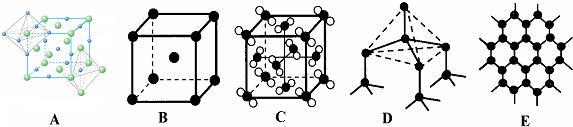
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{1}$H和${\;}_{1}^{2}$H互为同位素 | B. | 淀粉和纤维素互为同分异构体 | ||
| C. |  和 和 属于同一种物质 属于同一种物质 | D. | CH4和C2H6互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用热分解法从铁矿石中冶炼金属铁 | |
| B. | 用电解熔融氯化镁的方法获取金属镁 | |
| C. | 金属冶炼的过程是将金属从其化合物中还原出来 | |
| D. | 废旧金属的回收再利用有利于减轻污染、减少能耗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.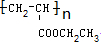 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解得到Cu的质量为3.2 g | |
| B. | 上述电解过程中共转移电子0.2 mol | |
| C. | 电解后的溶液中c(H+)=0.2 mol•L-1 | |
| D. | 原混合溶液中c(K+)=0.6 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com