
| A. | X的最高价氧化物对应的水化物是弱酸 | |
| B. | 元素Z位于元素周期表的第3周期Ⅵ族 | |
| C. | Y形成的单质能在二氧化碳中燃烧 | |
| D. | 原子半径的大小顺序:r(Z)>r(Y)>r(X) |
分析 短周期元素X、Y、Z的原子序数依次递增,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍,也是Y原子最外层电子数的3倍,最外层电子数不超过8个,K层不超过2个,则X内层电子数是2,所以X位于第二周期,Y、Z位于第三周期,则Z为S元素,Y最外层电子数为2,且处于第三周期,为Mg元素,这三种元素原子的最外层电子数之和为13,Y、Z最外层电子数之和为8,所以X最外层电子数为5,故X为N元素,据此解答.
解答 解:短周期元素X、Y、Z的原子序数依次递增,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍,也是Y原子最外层电子数的3倍,最外层电子数不超过8个,K层不超过2个,则X内层电子数是2,所以X位于第二周期,Y、Z位于第三周期,则Z为S元素,Y最外层电子数为2,且处于第三周期,为Mg元素,这三种元素原子的最外层电子数之和为13,Y、Z最外层电子数之和为8,所以X最外层电子数为5,故X为N元素.
A.X的最高价氧化物对应的水化物为硝酸,属于强酸,故A错误;
B.Z为S元素,位于元素周期表的第3周期ⅥA族,故B错误;
C.Mg能在二氧化碳中燃烧生成MgO与碳,故C正确;
D.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径r(Mg)>r(S)>r(N),故D错误,
故选C.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,需要学生熟练掌握核外电子排布,侧重考查分析、推断能力,难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:选择题
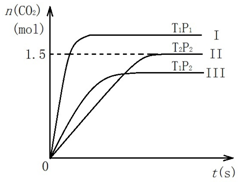 在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g).容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如图所示.以下说法合理的是( )
在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g).容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如图所示.以下说法合理的是( )| A. | 温度T2>T1 | B. | 压强P2>P1 | ||
| C. | II曲线表示NO平衡转化率为25% | D. | 该反应的焓变△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14 g C2H4中含有2NA个C-H键 | |
| B. | 1 mol•L-1 NH3•H2O溶液中含有NA个NH4+ | |
| C. | 1 mol Na2O2和足量CO2反应产生NA个O2分子 | |
| D. | 常温常压下,22.4 L 的SO2中含有NA个SO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
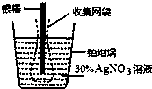 下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )| A. | 电量计工作时溶液里的阴离子向正极移动 | |
| B. | 电量计工作时银棒应与电源的正极相连 | |
| C. | 网袋是收集银溶解过程中产生的金属颗粒,若没有该网袋,测量结果会偏低 | |
| D. | 若得金属银的沉积量为1.08g,则电解过程中转移的电子为0.01mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H2S是一种弱电解质 | |
| B. | 可用石灰乳吸收H2S气体 | |
| C. | 根据如图可知FeCl3、CuCl2均能氧化H2S | |
| D. | H2S在空气中燃烧可以生成SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
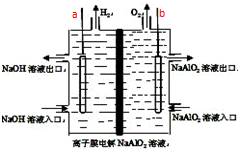 工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极):该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑.电解池阳极室发生的电极反应式是4AlO2-+6H2O-4e-=4Al(OH)3↓+O2↑,该离子膜为阳离子交换膜(填“阴”或“阳”)
工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极):该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑.电解池阳极室发生的电极反应式是4AlO2-+6H2O-4e-=4Al(OH)3↓+O2↑,该离子膜为阳离子交换膜(填“阴”或“阳”)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
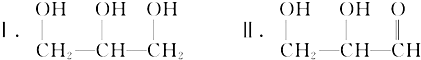
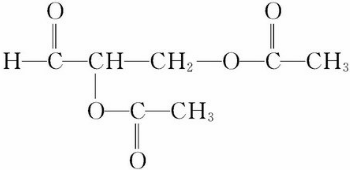 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
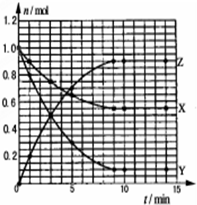 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )| A. | 反应的化学方程式是X+2Y?2Z | |
| B. | 该反应在0-3min时间内产物Z的平均反应速率0.083mol•L-1•min-1 | |
| C. | 由图象知该反应吸收能量 | |
| D. | 其他条件不变,升高温度,若正反应速率增大,则逆反应速率将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BOH溶于水,其电离方程式是BOH═B++OH- | |
| B. | 若将一定量的上述溶液混合后pH=7,则c(A- )=c(B+) | |
| C. | 在0.1 mol/L BA溶液中,c(B+)>c(A- )>c(OH- )>c(H+) | |
| D. | 若将0.1 mol/L BOH溶液稀释至0.001 mol/L,则溶液的pH=9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com