
| A、开启可乐瓶后,瓶中马上泛起大量泡沫 | B、对2HI?H2+I2(气)平衡体系增加压强使颜色变深 | C、反应CO+NO2?CO2+NO<0 升温使平衡向逆方向移动 | D、合成氨反应:N2+3H2?2NH3△H<0,为使氨的产率提高,理论上应采取低温高压的措施 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:三点一测丛书 高中化学(选修)化学反应原理 江苏版课标本 江苏版课标本 题型:013
|
从下列事实,找出不能用勒夏特列原理解释的是 | |
| [ ] | |
A. |
在溴水中存在如下平衡:Br2+H2O |
B. |
对2HI |
C. |
反应CO+NO2 |
D. |
合成氨反应:N2(气)+3H2(气) |
查看答案和解析>>
科目:高中化学 来源: 题型:
(08龙岩一中二模)从下列事实,找出不能用勒沙特列原理解释的是()
A.在溴水中存在如下平衡:Br2+H2O![]() HBr +HBrO,当加入NaOH溶液后颜色变浅
HBr +HBrO,当加入NaOH溶液后颜色变浅
B.对![]()
![]()
![]() 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深
C.反应CO+NO2![]() CO2+NO △H<0 升高温度使平衡向逆方向移动
CO2+NO △H<0 升高温度使平衡向逆方向移动
D.合成氨反应:N2+3H2![]() 2NH3 △H<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3 △H<0,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列事实,找出不能用勒沙特列原理解释的是( )
A.在溴水中存在如下平衡:![]() ,当加入NaOH溶液后颜色变浅
,当加入NaOH溶液后颜色变浅
B.对![]()
![]()
![]() 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深
C.反应![]()
![]()
![]() 升高温度使平衡向逆方向移动
升高温度使平衡向逆方向移动
D.合成氨反应:![]()
![]()
![]() ,为使氨的产率提高,理论上应采取低温高压的措施
,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省新余九中高二上学期期中考试化学试卷 题型:单选题
从下列事实,找出不能用勒沙特列原理解释的是
A.在溴水中存在如下平衡: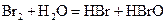 ,当加入NaOH溶液后颜色变浅 ,当加入NaOH溶液后颜色变浅 |
B.对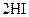  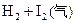 平衡体系增加压强使颜色变深 平衡体系增加压强使颜色变深 |
C.反应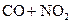  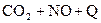 升高温度使平衡向逆方向移动 升高温度使平衡向逆方向移动 |
D.合成氨反应: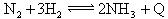 ,为使氨的产率提高,理论上应采取低温高压的措施 ,为使氨的产率提高,理论上应采取低温高压的措施 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com