
���� ��1���������м������BaCO3������NaOH��Һ��ʱ������������NaOH��Ӧ��ֻ��NaOH��ȫ��Ӧ��ʱ���������BaCO3��Ӧ����BaCO3���ܽ⣻
��2��ԭ��ҺΪ���ԣ���̪Ϊ��ɫ���ζ��յ�ʱ������ۺ������Ա仯���ʷ��յ㣬�յ�ӦΪdz��ɫ����ɫɫ��
��3����Ϊ�ζ����²���һ���̶ȣ�����ȷ�жϵζ������
��4�����ü�����ָʾ�����յ������ԣ�����NaOH�����ᷴӦ��BaCO3Ҳ�����ᷴӦ��
��� �⣺��1�����к͵��Ⱥ�˳���֪���������м������BaCO3������NaOH��Һ��ʱ������������NaOH��Ӧ��ֻ��NaOH��ȫ��Ӧ��ʱ���������BaCO3��Ӧ����BaCO3���ܽ⣬������ʹBaCO3�ܽ���ܲⶨNaOH�ĺ�����
�ʴ�Ϊ����Ϊ�μ�����������NaOH�����кͷ�Ӧ��
��2��ԭ��ҺΪ���ԣ�����̪Ϊ��ɫ���ζ��յ�ʱ����ɫ�仯Ϊdz��ɫ����ɫ��
�ʴ�Ϊ��dz��ɫ����ɫ��
��3����Ϊ�ζ����²���һ���̶ȣ��ʵ��ζ�Һ�������ʱ��������Һ�����С���ʲⶨ���ƫ�ͣ�����ȷ�жϵζ������
�ʴ�Ϊ�����ܣ�
��4�����ü�����ָʾ�����յ������ԣ�����NaOH�����ᷴӦ��BaCO3Ҳ�����ᷴӦ���ʲ�ѡ�����ã���ʹ������ƫ�࣬�ⶨ���ƫ�ߣ�
�ʴ�Ϊ�����ܣ� ƫ�ߣ�
���� ���⿼�����ʺ����ⶨ��Ϊ��Ƶ���㣬���յζ�ԭ����ʵ�������������ʹ��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע���к͵��Ⱥ�˳����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | Ũ�� | C�� | ѹǿ | D�� | �¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
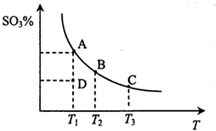 ��ҵ���������ж�������Ĵ�����ԭ��Ϊ2SO2��g��+O2��g���T2SO3��g������Ӧ�����ϵ��ƽ��״̬ʱSO3�İٷֺ������¶ȵĹ�ϵ��ͼ��ʾ������˵��������ǣ�������
��ҵ���������ж�������Ĵ�����ԭ��Ϊ2SO2��g��+O2��g���T2SO3��g������Ӧ�����ϵ��ƽ��״̬ʱSO3�İٷֺ������¶ȵĹ�ϵ��ͼ��ʾ������˵��������ǣ�������| A�� | ��A��B��C����ʱ��v������=v���棩����D��ʱv��������v���棩 | |
| B�� | A��B��C�����ƽ�ⳣ��һ������ͬ | |
| C�� | �����¶ȿ��Լӿ컯ѧ��Ӧ���ʣ�������ƽ��������Ӧ�����ƶ� | |
| D�� | ��һ���¶��£���������������䣬��ƽ����ϵ��ͨ��ϡ�����壬ѹǿ����ƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 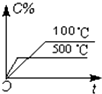 | B�� | 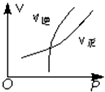 | C�� | 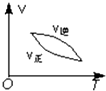 | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
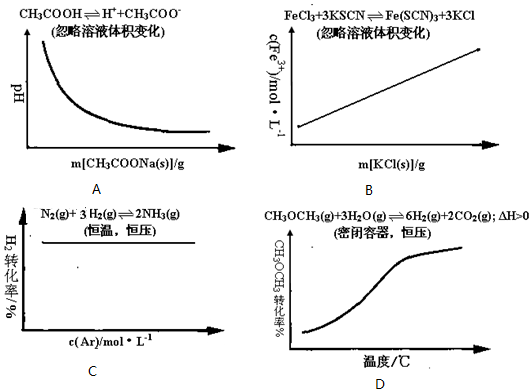
| A�� | ��100mL 0.1mol/L������Һ����������ƾ����������ҺpH�ı仯����ͼ | |
| B�� | ��FeCl3��Һ��KSCN��Һ��Ϻ�Ӧ��ƽ�������Һ���������KCl������c��Fe3+���ı仯����ͼ | |
| C�� | �ܱ������н���N2��g��+3H2��g��?2NH3��g����Ӧ�ﵽƽ����ֺ��º�ѹ�����£���ͨ��ϡ������Ar�Ĺ�����H2��ת���ʱ仯����ͼ | |
| D�� | �ܱ������н���CH3OCH3��g��+3H2O��g��?6H2��g��+2CO2��g����H��0�ﵽƽ����ֺ�ѹ�����£��������¶ȹ�����CH3OCH3��ת���ʱ仯����ͼ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com