
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
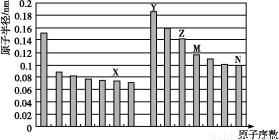
A.N、Z两种元素的离子半径相比前者较大
B.M、N两种元素的气态氢化物的稳定性相比后者较强
C.X与M两种元素组成的化合物能与碱反应,但不能与任何酸反应
D.工业上常用电解Y和N形成的化合物的熔融态制取Y的单质
科目:高中化学 来源:2014高考化学名师选择题专练 离子反应练习卷(解析版) 题型:选择题
室温时,下列各组离子在指定溶液中可以大量共存的是( )
A.由水电离出的c(H+)=10-12 mol/L的溶液中:Na+、Ba2+、HC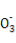 、C1-
、C1-
B.无色透明溶液中:K+、Cu2+、S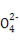 、Na+
、Na+
C.含有大量Al 的溶液中:Na+、OH-、Cl-、C
的溶液中:Na+、OH-、Cl-、C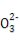
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、S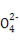
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
某新型碱性可充电电池,能长时间保持稳定的放电电压。该电池的总反应为3Zn+2K2FeO4+8H2O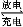 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
A.电池放电是化学能转化成电能的过程
B.放电时正极反应为:Fe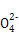 +4H2O+3e-
+4H2O+3e-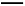 Fe(OH)3+5OH-
Fe(OH)3+5OH-
C.充电时电池的负极接外电源的正极
D.充电时电解质溶液中的阴离子向阳极定向移动
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学与STSE练习卷(解析版) 题型:选择题
下列叙述不正确的是( )
A.“海沙危楼”是由于海沙带有腐蚀性,会腐蚀混凝土中的钢筋等
B.食用地沟油对人体危害极大,是因为含有黄曲霉素等有毒物质
C.开发利用太阳能、风能、生物能、海洋能等清洁能源,符合“低碳经济”
D.光化学烟雾、温室效应、硝酸型酸雨的形成都只与氮氧化物有关
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
元素编号 | 元素性质或原子结构 |
X | 形成的简单阳离子核外无电子 |
Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
Z | 元素在周期表的族序数等于周期序数的3倍 |
T | 同周期元素中形成的简单离子半径最小 |
下列说法正确的是( )
A.原子半径大小顺序:T>Z>Y>X
B.常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液反应生成氢气
C.X分别与Y、Z均可形成既含极性键又含非极性键的化合物
D.由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.0.5 mol O3与11.2 L O2所含的分子数一定相等
B.常温常压下,78 g Na2O2和Na2S的混合物中含有的阴离子数为NA
C.2SO2(g)+O2(g)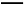 2SO3(g)和SO2(g)+
2SO3(g)和SO2(g)+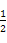 O2(g)
O2(g)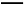 SO3(g)的ΔH相等
SO3(g)的ΔH相等
D.物质的量浓度为0.25 mol/L的MgCl2溶液中,含有Cl-个数为0.5NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.在0 ℃时,22.4 L氢气中含有2NA个氢原子
B.电解食盐水若产生2 g氢气,则转移的电子数目为NA
C.1 mol乙烷分子中共价键总数为7NA
D.密闭容器中46 g NO2含有的分子数为NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质性质综合应用练习卷(解析版) 题型:填空题
磷酸铁锂(LiFePO4)被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下:
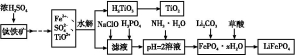
已知:H2TiO3是种难溶于水的物质。
(1)钛铁矿用浓硫酸处理之前,需要粉碎,其目的是 。
(2)TiO2+水解生成H2TiO3的离子方程式为 。
(3)加入NaClO发生反应的离子方程式为 。
(4)在实验中,从溶液中过滤出H2TiO3后,所得滤液浑浊,应如何操作 。
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁已全部转化为二价铁离子),采取KMnO4标准液滴定Fe2+的方法:(不考虑KMnO4与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果 (填“偏高”、“偏低”或“无影响”),滴定终点的现象是 。滴定分析时,称取a g钛铁矿,处理后,用c mol/L KMnO4标准液滴定,消耗V mL,则铁元素的质量分数的表达式为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 选修2化学与技术练习卷(解析版) 题型:选择题
在接触法产生H2SO4的过程中,对“废气、废水、废渣、废热”的处理正确的是( )
①废气用氨水处理 ②污水用石灰乳处理 ③废渣用来造水泥或炼铁 ④设置“废热”锅炉产生蒸气来供热或发电
A.只有①② B.只有①③④ C.只有①②③ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com