
| A. | 原子半径:M>Y | B. | 对应氢化物的沸点:M>Z | ||
| C. | 对应氢化物的稳定性:X>Y | D. | XY2与MY2溶于水都能得到对应的酸 |
分析 X、Y、Z、M为原子序数依次增大的4种短周期元素,Y与其同主族的短周期元素可形成一种常见的气体,则Y为氧,生成的气体为二氧化硫,所以X为氮元素,Z为氟元素,M原子的核外电子数是Z原子最外层电子数的2倍,则M为14号元素,硅元素,据此答题.
解答 解:X、Y、Z、M为原子序数依次增大的4种短周期元素,Y与其同主族的短周期元素可形成一种常见的气体,则Y为氧,生成的气体为二氧化硫,所以X为氮元素,Z为氟元素,M原子的核外电子数是Z原子最外层电子数的2倍,则M为14号元素,硅元素,
A、电子层数越多,半径越大,所以原子半径:Si>O,故A正确;
B、由于HF能形成氢键,所以SiF的氢化物沸点低于HF,SiH4<HF,故B错误;
C、非金属性越强,对应的氢化物越稳定,所以Y的氢化物稳定性大于X,故C错误;
D、二氧化硅不溶于水,故D错误;
故选A.
点评 本题考查结构性质位置关系应用,难度中等,推断元素是解题关键,注意二氧化硅与水不能反应,为易错点,注意对元素周期律的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 3.36 L | B. | 6.72 L | ||
| C. | 大于3.36 L,小于5.60 L | D. | 大于5.60 L,小于6.72 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | B. | CH2=CH2+Br2→CH2BrCH2Br | ||
| C. | 2C2H5OH+2Na→2C2H5ONa+H2↑ | D. | 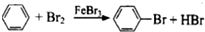 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
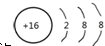 ,A2C2的结构式:H-O-O-H.
,A2C2的结构式:H-O-O-H.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装置 |  | 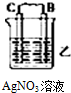 | 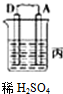 |
| 现象 | 金属A不断溶解 | C极质量增加 | A上有气体产生 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键只存在于分子之间 | |
| B. | 化学键只存在于离子之间 | |
| C. | 化学键是相邻的原子或离子之间强烈的相互作用 | |
| D. | 化学键是相邻的分子之间强烈的相互作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 65 mL 2mol/L的NaCl溶液 | B. | 25 mL 2mol/L的MgCl2溶液 | ||
| C. | 10 mL 2mol/L的AlCl3溶液 | D. | 50 mL 2mol/L的kCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com