

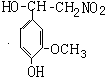
 ,
, 反应生成A,A和氢气加成生成
反应生成A,A和氢气加成生成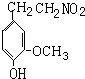 ,将
,将 和
和 比较知,
比较知, 先发生消去反应生成A,A再和氢气发生加成反应生成
先发生消去反应生成A,A再和氢气发生加成反应生成 ,所以A的结构简式为
,所以A的结构简式为 ,
, 和Zn、HCl发生还原反应生成
和Zn、HCl发生还原反应生成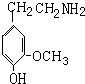 ,
,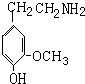 发生水解(取代)反应生成多巴胺,据此答题.
发生水解(取代)反应生成多巴胺,据此答题. ,
, 反应生成A,A和氢气加成生成
反应生成A,A和氢气加成生成 ,将
,将 和
和 比较知,
比较知, 先发生消去反应生成A,A再和氢气发生加成反应生成
先发生消去反应生成A,A再和氢气发生加成反应生成 ,所以A的结构简式为
,所以A的结构简式为 ,
, 和Zn、HCl发生还原反应生成
和Zn、HCl发生还原反应生成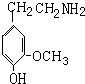 ,
,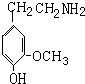 发生水解(取代)反应生成多巴胺,
发生水解(取代)反应生成多巴胺, ,可知,香兰素中除了醛基之外,香兰素还含有羟基、醚键,故答案为:羟基、醚键;
,可知,香兰素中除了醛基之外,香兰素还含有羟基、醚键,故答案为:羟基、醚键; 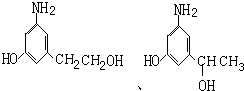 ,
,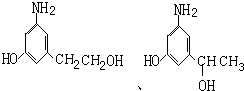 (其中之一);
(其中之一); ,A与足量浓溴水反应的化学方程式为
,A与足量浓溴水反应的化学方程式为 ,
, .
.


科目:高中化学 来源: 题型:
| A、C4H8可能是烯烃 |
| B、C4H8中属于烯烃类的同分异构体有4种 |
C、核磁共振氢谱有2种吸收峰的烯烃结构一定是 |
| D、C4H8中属于烯烃的顺反异构体有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、1 mol N2(g)与1 mol O2(g)反应放出的能量为180 kJ |
| B、1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的能量 |
| C、通常情况下,N2(g)与O2(g)混合能直接生成NO(g) |
| D、N2的燃烧热△H=-180 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol CH4在足量的氧气中充分燃烧生成稳定的氧化物的燃烧热为-1780.6 kJ?mol-1 |
| B、2 mol CH4在足量的氧气中充分燃烧生成CO2(g)和H2O(g)的燃烧热为-890.3 kJ?mol-1 |
| C、1 L 0.1 mol?L-1 NaOH溶液与1 L 0.1 mol?L-1 HCl溶液反应的中和热为-57.3 kJ?mol-1 |
| D、2 L 1 mol?L-1 NaOH溶液与1 L 1 mol?L-1 H2SO4溶液反应的反应热为-57.3 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 25℃时,已知某些物质的电离平衡常数如表:
25℃时,已知某些物质的电离平衡常数如表:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、3:3:3 |
| B、3:2:1 |
| C、1:1:1 |
| D、3:2:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com