
����Ŀ��[��ѧ��ѡ��2����ѧ�뼼��]
��ҵ��ͭ�ķ������ɻ�ͭ������Ҫ�ɷ���CuFeS2,���ʲ���ͭԪ�������ƾ�ͭ�Ĺ�������ʾ��ͼ��ͼ��

��1������ͭ����ͭ����������Ϊ0.4������1�ִ�ͭ��������Ҫ���ֻ�ͭ��____________�֡�
��2�����ڷ���¯�У���ͭ����ɰ��ʯӢɰ��ϼ��ȵ�1000�����ң���ͭ���������Ӧ����Cu��Fe�ĵͼ����_____________________���Ҳ���Fe������ת��ΪFe�ĵͼ������
��3�����ӻ��������ͳ������ԭ�ϽǶȿ���δ��������ò�����������___________��
��4������ת¯�У���ͭ�е�Cu2S�ȱ�������Cu2O��,���ɵ�Cu2O����Cu2S��Ӧ��������Ӧ���Ȼ�ѧ����ʽΪ����2Cu2S��s��+3O2��g���T2Cu2O��s����+2SO2��g����H=-768.2kJ.mol-1
��2Cu2O��s��+Cu2S��s���T6Cu��s��+SO2��g����H=+116.0kJ.mol-1
��ӦCu2Sת��Ϊͭ���Ȼ�ѧ����ʽ��_________________________��
��3molCu2S��һ�����Ŀ����������������������Ϊ4:1�����ܱ������г�ַ�Ӧ�����������Ӧ����ȫ��Cu2S��ȫ���뷴Ӧ�����õ�����ͭ3mol������������SO2���������Ϊ_____________��
��5������⾫��ͭ���������ҺΪ______________�����һ��ʱ��������Һ��Ũ��_____________������������������������������������
��6�������ڷ�ӦCu+H2O2+H2SO4=CuSO4+2H2O�����Ʊ�CuSO4�������÷�Ӧ���Ϊԭ��أ��������缫��ӦʽΪ__________________��
���𰸡���1����2.5t��2����
��2����2CuFeS2+O2![]() Cu2S+2FeS+SO2��2����
Cu2S+2FeS+SO2��2����
��3�����ð�ˮ���������е�SO2������NH4��2SO3��NH4HSO3���������ɵ���NH4��2SO3��NH4HSO3�����ᷴӦ����SO2���ռ�SO2��������H2SO4
��4����Cu2S��s��+O2��g��=2Cu��s��+SO2��g����H=-217.4kJ.mol-1��2����16.7%��2����
��5����CuSO4Cu��NO3��2��1����,������2������6����H2O2+2H++2e-=2H2O��2����
��������
�����������1����ͭ����ͭ����������Ϊ0.4������1�ִ�ͭ��������Ҫ���ֻ�ͭ��������Ϊ![]() ��
��
��2��.�ڷ���¯�У���ͭ����ɰ��ʯӢɰ��ϼ��ȵ�1000�����ң���ͭ���������Ӧ����Cu��Fe�ĵͼ����������������ͭ�����������Ҳ���Fe������ת��ΪFe�ĵͼ���������������SO2���ɣ���Ӧ�ķ���ʽΪ2CuFeS2+O2![]() Cu2S+2FeS+SO2��
Cu2S+2FeS+SO2��
��3��.��������Ҫ�ɷ��Ƕ����������ӻ��������ͳ������ԭ�ϽǶȿ������ķ������ð�ˮ���������е�SO2������NH4��2SO3��NH4HSO3���������ɵ���NH4��2SO3��NH4HSO3��
��4����֪����2Cu2S��s��+3O2��g���T2Cu2O��s����+2SO2��g����H=-768.2kJ.mol-1
��2Cu2O��s��+Cu2S��s���T6Cu��s��+SO2��g����H=+116.0kJ.mol-1
�����ݸ�˹���ɿ�֪����+������3���õ���ӦCu2Sת��Ϊͭ���Ȼ�ѧ����ʽΪCu2S��s��+O2��g����2Cu��s��+SO2��g����H=-217.4kJ.mol-1��
��3molCu2S��һ�����Ŀ����������������������Ϊ4:1�����ܱ������г�ַ�Ӧ�����������Ӧ����ȫ��Cu2S��ȫ���뷴Ӧ�����õ�����ͭ3mol����
2Cu2S+3O2��2Cu2O+2SO2
2.5mol 3.75mol 2.5mol 2.5mol
Cu2S+2Cu2O��6Cu+SO2��
0.5mol 1mol 3mol 0.5mol
��Ӧ��������Ϊ3.75mol�����������ʵ�����������4�������������ʵ���Ϊ15mol�����ɵĶ�������Ϊ3mol�������������еĶ���������������![]() ��100%=16.7%��
��100%=16.7%��
��5����⾫��ͭʱ�������ҺΪCuSO4�����ڴ�ͭ�к������ʣ�����Ҳʧȥ���ӣ���˵��һ��ʱ��������Һ��Ũ�ȼ��١�
��6�����ڷ�ӦCu+H2O2+H2SO4=CuSO4+2H2O�����Ʊ�CuSO4�������÷�Ӧ���Ϊԭ��أ��������缫��˫��ˮ�õ����ӣ��������缫��ӦʽΪH2O2+2H++2e-=2H2O��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������1807�껯ѧ�Ҵ�ά�õ���������������Ƶ��ƣ���Ӧԭ��Ϊ��4NaOH��������=4Na+O2��+2H2O���������� ����������������������������Ҳ�Ƶ��ƣ���Ӧԭ��Ϊ��3Fe+4NaOH=Fe3O4+2H2��+4Na���������й�˵����ȷ������ ��
A��������������������ƣ����������缫��ӦΪ��Na++e-=Na
B�����������˷�����ԭ�����������Ļ�ԭ�Ա���ǿ
C������ά������������˷��Ƶõ������ƣ�������Ӧ��ת�Ƶĵ���������Ϊ2:l
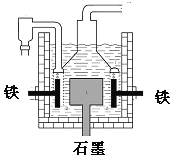
D��Ŀǰ��ҵ�ϳ��õ�������Ȼ��Ʒ���������ͼ����������ʯī��Ϊ��������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a��b��c��d��e�ֱ���Cu��Ag��Fe��Al��Mg���ֽ����е�һ�֡���֪����a��c������ϡ���ᷴӦ�ų����壻��b��d�������η�Ӧ���û�������d����c��ǿ�Ӧ�ų����壻��c��e�����Ũ�����з����ۻ����ɴ��жϣ�a��b��c��d��e�ֱ���( )
A��Fe��Cu��Al��Ag��Mg B��Al��Cu��Mg��Ag��Fe
C��Mg��Cu��Al��Ag��Fe D��Mg��Ag��Al��Cu��Fe
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��ֻ���ܺ���H+��NH4+��Mg2+��Al3+��Fe3+��CO32-��SO42-��NO3-�еļ��֣���������п����������ɫ��ζ�����壻��������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ��������˵����ȷ������ ��

A����Һ�е�������ֻ��H+��Mg2+��Al3+���ܺ���Fe3+
B����Һ��һ������CO32-��NO3-��һ������SO42-
C����Һ��c��NH4+��=0.3 mol/L
D��c��H+����c��Al3+����c��Mg2+��=1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NO2��SO2��CO���Ǵ�����Ⱦ�����˵����ȷ����( )
A��NO2��SO2������������
B��NO2��SO2���Ի��գ��ֱ���Ϊ�Ʊ����ᡢ�����ԭ������CO�ɻ�����Ϊȼ����
C�����߾������������Ԫ�صĵ��ʻ��϶���
D��������Ⱦ�����嶼�����ü�Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ���Ũ��Ϊ0.1 mol/L��Na2CO3��Һl00mLʱ�����в�����ȷ����( )
A. ��������ƽ��ȡl.06g��ˮ̼���ƣ����ձ��м�����ˮ�ܽ⣬����ȴ�����º���Һת�Ƶ�����ƿ��
B. ����ʱ�������ӣ���������Һ��Ũ�Ƚ�ƫ��
C. ����ʱ������ˮ�����̶��ߣ����ý�ͷ�ι�С���������ಿ��
D. ��ʹ������ƿǰ����������ƿ�Ƿ�����Լ�ƿ�����Ƿ�©ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Լ���ŵ�������ȷ����( )

A. Ũ�����װ�˰�װ��Ӧ������ͼ��ʾ�ı�־
B. �����Ʊ�����CCl4��(�Ƶ��ܶ�С��CCl4)
C. ����������Һ�����ڴ��������IJ���ƿ��
D. ��������Һ�������ɫ�Լ�ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� Fe��Mg��H2SO4��Ӧ��ʵ�����£�
ʵ�� |
|
|
|
|
���� | Fe�������������ɫ���� | Fe����������ݺ�Ѹ��ֹͣ | Mg����Ѹ�ٲ����������� | Fe�����д������ݣ�Mg�������������� |
��������ʵ��˵�������������� ��
A��I�в��������ԭ���ǣ�Fe + 2H��=Fe2��+ H2��
B��ȡ�����е���������CuSO4��Һ������������ɫ����
C����������˵��Mg��ŨH2SO4��û���ۻ�
D����������˵��Mg�Ľ����Ա�Feǿ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com