
【题目】根据下列的有机物合成路线回答问题: 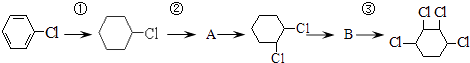
(1)写出A、B的结构简式:A、B .
(2)写出各步反应类型:①②③ .
(3)写出②、③的反应方程式: ② ,
③ .
【答案】
(1)![]() ;
;![]()
(2)加成反应;消去反应;加成反应
(3)![]() +NaOH
+NaOH ![]()
![]() +NaCl+H2O;
+NaCl+H2O;![]() +2Cl2→
+2Cl2→ ![]()
【解析】解:由合成路线分析可知,采用逆推法,则B应为 ![]() ,所以反应③为B与氯气加成反应,由
,所以反应③为B与氯气加成反应,由 ![]() 可以B反推得A为
可以B反推得A为 ![]() ,所以反应②为消去反应,氯苯与氢气发生加成反应生成
,所以反应②为消去反应,氯苯与氢气发生加成反应生成 ![]() ,(1)根据以上分析,A、B的结构简式分别为:
,(1)根据以上分析,A、B的结构简式分别为: ![]() 、
、 ![]() ,所以答案是:
,所以答案是: ![]() ;
; ![]() ;(2)根据以上分析,①为加成反应,②为消去反应,③加成反应,所以答案是:加成反应;消去反应;加成反应;(3)反应②的化学方程式为
;(2)根据以上分析,①为加成反应,②为消去反应,③加成反应,所以答案是:加成反应;消去反应;加成反应;(3)反应②的化学方程式为 ![]() +NaOH
+NaOH ![]()
![]() +NaCl+H2O,反应③的化学方程式为
+NaCl+H2O,反应③的化学方程式为 ![]() +2Cl2→
+2Cl2→ 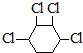 ,所以答案是:
,所以答案是: ![]() +NaOH
+NaOH ![]()
![]() +NaCl+H2O;
+NaCl+H2O; ![]() +2Cl2→
+2Cl2→  .
.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】下列关于Fe(OH)3胶体的制备,正确的操作是( )
A. 将FeCl3 溶液滴入热水中,得到黄色液体即可
B. 将FeCl3 溶液滴入蒸馏水中即可
C. 将饱和FeCl3 溶液滴入沸水中,并继续加热煮沸得到红褐色液体即可
D. 将饱和FeCl3 溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀即可
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1mol.
(1)烃A的分子式为 .
(2)若烃A不能使溴水褪色,但在一定条件下,能与Cl2发生取代反应,其一氯代物只有一种,则A的结构简式为 .
(3)若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物分子中含有3个甲基,则A所有可能的结构简式为 , , .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所述的操作中没有涉及到化学变化的是
A.豆科作物的根瘤菌对空气中氮的固定B.将NO2气体冷却后颜色会变浅
C.通过煤的液化来提取苯、二甲苯等化工原料D.工业制液态氧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤脱硫可减少SO2尾气的排放,燃煤脱硫技术受到各界科研人员的关注.一种燃煤脱硫技术的原理是:CaO(s)+3CO(g)+SO2(g)CaS(s)+3CO2(g)△H=﹣394.0kJ/mol.保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):下列有关说法正确的是( ) 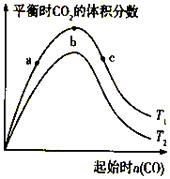
A.T1比T2高
B.b点SO2转化率最高
C.b点后曲线下降是因CO体积分数升高
D.减小压强可提高CO,SO2转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果:
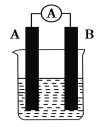
实验序号 | A | B | 烧杯中的液体 | 灵敏电流表指针是否偏转 |
1 | Zn | Zn | 乙醇 | 无 |
2 | Zn | Cu | 稀硫酸 | 有 |
3 | Zn | Cu | 稀硫酸 | 无 |
4 | Zn | Cu | 苯 | 无 |
5 | Cu | C | 氯化钠溶液 | 有 |
6 | Mg | Al | 氢氧化钠溶液 | 有 |
分析上述实验,回答下列问题:
(1)实验2中电流由________极流向________极(填“A”或“B”)。
(2)实验6中电子由B极流向A极,表明负极是________(填“镁”或“铝”)电极。
(3)实验5表明________(填字母序号,下同)。
A.铜在潮湿空气中不会被腐蚀
B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确的是________。
A.金属活动顺序表中,活泼性强的金属一定作负极
B.失去电子的电极是负极
C.烧杯中的液体必须是电解质溶液
D.原电池中,浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) ![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
A.550℃时,若充入惰性气体,正,逆 均减小,平衡不移动
B.650℃时,反应达平衡后CO2的转化率为25.0%
C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0p总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在80 ℃时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4![]() 2NO2 ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
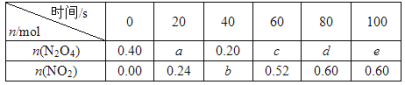
(1)计算20~40 s内用N2O4表示的平均反应速率为_________mol/( L s)。
(2)计算在80℃时该反应的平衡常数K=__________(请注明单位)。
(3)反应进行至100 s后将反应混合物的温度降低,混合气体的颜色______(填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有_________(填序号)。
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
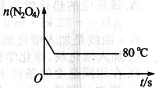
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com