
| A. | CuSO4水溶液 | B. | 银氨溶液 | C. | 硫氰化铁溶液 | D. | I2的CCl4溶液 |
分析 配离子是由一个金属阳离子和一定数目的中性分子或阴离子以配位键结合而成的复杂离子,可能存在于配位化合物晶体中,也可能存在于溶液中,据此解答.
解答 解:A.水对铜离子有络合作用,CuSO4水溶液中存在四水合铜络离子,铜离子提供空轨道,水分子提供孤对电子,存在配离子,故A不选;
B.银氨溶液中银离子提供空轨道,氨气提供孤对电子,存在配离子,故B不选;
C.硫氰化铁溶液中铁离子提供空轨道,硫氰根离子提供孤对电子,存在配离子,故C不选;
D.I2的CCl4溶液为碘单质的四氯化碳溶液,无配离子,故D选;
故选D.
点评 本题考查配离子,题目难度中等,注意配离子可能存在于配位化合物晶体中,也可能存在于溶液中,把握相关概念是解答的关键.


科目:高中化学 来源: 题型:选择题
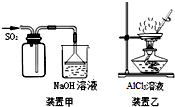
| A. | 用装置甲收集SO2 | |
| B. | 用装置乙制备AlCl3晶体 | |
| C. | 中和滴定时,锥形瓶用待装液润洗 | |
| D. | 使用分液漏斗和容量瓶时,先要检查是否漏液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
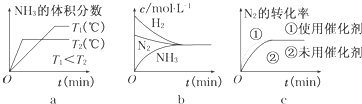
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为14的碳原子的表达式:${\;}_{8}^{14}$C | |
| B. | 乙醇的结构简式:C2H5OH | |
| C. | 乙烯的结构简式为CH2CH2 | |
| D. | 甲烷分子的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
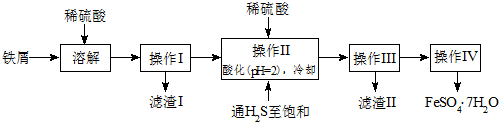
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 1:3:2 | C. | 2:3:1 | D. | 3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 L 3mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3NA | |
| B. | 1mol金刚石中含有的共价键数目为4NA | |
| C. | 1molNa2O2与足量的水反应,转移的电子数为2NA | |
| D. | 分子数为NA的CO、N2的混合气体在标准状况时体积约为22.4L,质量为28g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HCl | B. | Na2CO3 | C. | NaCl | D. | KOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com