
| A�� | �Ҵ�������������Һ�����Խ������������ﵽ������Ŀ�� | |
| B�� | ���������Һ��˫��ˮ������ԭ����ͬ | |
| C�� | ˫��ˮ���н�ǿ�ĸ�ʴ�ԣ�����������ϴ���� | |
| D�� | �ڴ���������Һ��ͨ��������������ɵõ��������ƺʹ����� |
���� A���Ҵ�ʹ�����ʱ��ԣ�
B�����������Һ��˫��ˮ������ǿ�����ԣ�
C�������Կ�����������
D���ڴ���������Һ��ͨ����������������������ԭ��Ӧ��
��� �⣺A���Ҵ�����Һ��������Ϊ����ʹ�����ʱ��ԣ��������ǽ�����������������������Һ���Խ������������ﵽ������Ŀ�ģ���A����
B�����������Һ��˫��ˮ������ԭ��������Ϊ����ǿ�����ԣ�ԭ����ͬ����B��ȷ��
C��˫��ˮ���н�ǿ�������ԣ�������Ƥ������������C����
D������������Һ��ͨ��������������������������Ӻ�ˮ����D����
��ѡB��
���� ���⿼��±��Ԫ�ؼ�����������ʣ�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ����������;�Ĺ�ϵΪ���Ĺؼ������ط���Ӧ�������Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
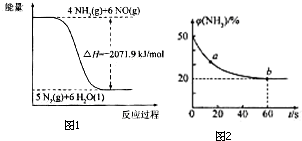 ����Ӧ�úʹ������Ļ��������������������Ҫ���壮
����Ӧ�úʹ������Ļ��������������������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al 1s22s22p63s23p1 | B�� | O2-��1s22s22p4 | ||
| C�� | Na��1s22s22p63s1 | D�� | F��1s22s22p5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| c��HCO3-����c��H2CO3�� | 1.0 | 17.8 | 20.0 | 22.4 |
| PH | 6.10 | 7.35 | 7.40 | 7.45 |
| A�� | pH=7.30��ѪҺ�У�HCO3-��ˮ��̶�һ������H2CO3�ĵ���̶� | |
| B�� | ����ѪҺ���ж�ʱ����ע��NaHCO3��Һ���� | |
| C�� | pH=7.00��ѪҺ�У�c��H2CO3����c��HCO3-�� | |
| D�� | ��������ѪҺ�У�HCO3-��ˮ��̶ȴ������ĵ���̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | �������ʵ | ���� |
| A | �����½�AlƬ����Ũ�����������Ա仯 | Al��Ũ�����Ӧ |
| B | ���ȵ��з�̪�Ĵ�������Һ����Һ��ɫ���� | ���ȴٽ�CH3COO-ˮ�⣬��Һ�ļ�����ǿ |
| C | ����ˮ�ֱ����ֲ���ͺ��ѻ������У���ˮ����ɫ | ǰ��������ȡ����ɫ���������ڷ����ӳɷ�Ӧ����ɫ |
| D | ����NaHCO3��Һ�����Ա仯 | NaHCO3�����ȶ���ǿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

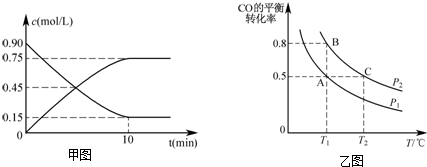
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
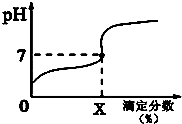 �����£���0.1000mol/L��NaOH��Һ�ζ�20mlͬŨ�ȵ�һԪ����HA���ζ�������ҺpH��X�ı仯������ͼ��ʾ�������к���ЧӦ��������˵������ȷ���ǣ�������
�����£���0.1000mol/L��NaOH��Һ�ζ�20mlͬŨ�ȵ�һԪ����HA���ζ�������ҺpH��X�ı仯������ͼ��ʾ�������к���ЧӦ��������˵������ȷ���ǣ�������| A�� | HA��Һ��ˮϡ�ͺ���Һ��$\frac{c��HA��}{c��{A}^{-}��}$��ֵ��С | |
| B�� | HA�ĵ��볣��KHA=$\frac{1{0}^{-7}X}{100-X}$��xΪ�ζ������� | |
| C�� | ���ζ�����Ϊ100ʱ����Һ��ˮ�ĵ���̶���� | |
| D�� | �ζ���������100ʱ����Һ������Ũ�ȹ�ϵһ����c��Na+����c��A-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��KMnO4��H+����Һ����ױ�����ϩ������ | |
| B�� | ����ˮ���𱽡���ϩ�����Ȼ�̼ | |
| C�� | ��ˮ�����Ҵ����������Ȼ�̼ | |
| D�� | ��NaOH��Һ���𱽷���Һ���ױ��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com