
| A. | SiC是一种新型无机非金属材料,任何条件下都不可能在空气中燃烧 | |
| B. | 制造粗硅时的反应:2SiO2+5C$\frac{\underline{\;高温\;}}{\;}$Si+SiC+4CO↑ | |
| C. | Si、SiO2能用NaOH溶液分离 | |
| D. | 纯净的SiO2只能用于制造光导纤维 |
分析 反应的方程式为2SiO2+5C$\frac{\underline{\;高温\;}}{\;}$Si+SiC+4CO↑,该反应中C元素化合价由0价变为-4价、+2价,Si化合价由+4价降低到0价,O元素化合价不变,以此解答该题.
解答 解:A.根据SiC中C可以失电子,具有还原性,高温下能在空气中燃烧生成SiO2和CO2,故A错误;
B.粗硅中含有SiC,其中Si和SiC的物质的量之比为1:1,根据原子守恒,可写出化学方程式:2SiO2+5C$\frac{\underline{\;高温\;}}{\;}$Si+SiC+4CO↑,故B正确;
C.Si、SiO2均能与NaOH溶液反应,不能用NaOH溶液分离,故C错误;
D.纯净的SiO2除了制造光导纤维,还可用于制造光学玻璃等,故D错误.
故选B.
点评 本题考查氧化还原反应,侧重于学生的分析能力和基本概念的理解和应用的考查,为高频考点,难度不大,注意从元素化合价的角度认识和解答该类题目.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+CO2═2Na2CO3+O2 | B. | 2Na2O2+2SO3═2Na2SO4+O2 | ||
| C. | Na2O2+H2SO4═Na2SO4+H2O2 | D. | 3Na2O2+Cr2O3═2Na2CrO4+Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素原子最外层电子数越多,元素金属性越强 | |
| B. | 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 | |
| C. | Si、P、S、Cl元素的单质与氢气化合越来越容易 | |
| D. | F-、O2-、Mg2+、Na+离子半径逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 | |
| B. | 除短周期外,其它周期均为18种元素 | |
| C. | 乙元素的族序数比甲元素的族序数小 | |
| D. | 甲、丙元素最高价氧化物对应水化物的酸性强弱:甲<丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备其单质 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
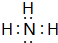 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①③⑤ | C. | ②④⑧ | D. | ①⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
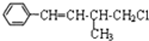
| A. | 1mol该有机物在加热和催化剂作用下,最多能和4molH2反应 | |
| B. | 该有机物分子式为C11H13Cl | |
| C. | 该有机物遇硝酸银溶液产生白色沉淀 | |
| D. | 该有机物在一定条件下,能发生消去反应或取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com