
| A、在河流人海口处易形成三角洲 |
| B、在NaHCO3溶液中滴入CaCl2溶液,看不到沉淀 |
| C、少许FeCl3饱和溶液逐滴滴入沸水中,看不到红褐色沉淀 |
| D、同一支钢笔,同时使用不同牌号的墨水易发生堵塞 |


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案科目:高中化学 来源: 题型:
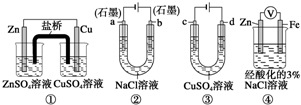
| A、装置②工作一段时间后,a极附近溶液的pH增大 |
| B、用装置③精炼铜时,c极为粗铜 |
| C、装置①中,盐桥中的K+移向ZnSO4溶液 |
| D、装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b | B、a<b |
| C、a=b | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| B、KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀2Al3++3 SO42-+3 Ba2++6 OH-=2Al(OH)3↓+3BaSO4↓ |
| C、将少量硝酸银溶液滴入氨水中:Ag++2NH3?H2O═[Ag(NH3)2]++2H2O |
| D、碳酸氢钠溶液中加入过量的石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得 |
| B、金属与盐溶液反应都是置换反应 |
| C、液氨、液氯、液态氯化氢都是非电解质 |
| D、凡能电离出氢离子的化合物都是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
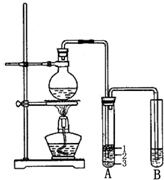 实验室制取少量溴乙烷的装置如图所示.
实验室制取少量溴乙烷的装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
2- 8 |
2- 4 |
- 4 |
2- 8 |
2- 8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com