
【选修3:物质结构与性质】
东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电子排布式为___________,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是___________
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。 在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为___________,提供孤电子对的成键原子是___________。金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n ,推测Ni(CO)n的晶体类型为___________;与Ni(CO)n中配体互为等电子体的离子的化学式为___________(写出一个即可).
(3)单质铜及镍都是由___________键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol– 1、INi=1753 kJ·mol– 1,ICu> INi的原因是____________。
(4)某铜金合金晶体具有面心立方最密堆积的结构.在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为_____________,若该晶胞的边长为a cm,则合金的密度为_____________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | 若在阴极附近的溶液中滴入紫色石蕊试液,溶液呈红色 | |
| B. | 若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 | |
| C. | 电解时在阳极得到氯气,在阴极得到金属钠 | |
| D. | 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液变回NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:H2>Li | B. | H-与Li+的电子层结构相同 | ||
| C. | 微粒半径:r(H-)>r(H)>r(H+) | D. | LiH属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:选择题
下列实验操作及现象与实验结论一致的是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中不一定含有SO42- |
B | 光洁的铁钉放在冷的浓硫酸中,无明显现象 | 铁钉与冷的浓硫酸不反应 |
C | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡静置,下层分别呈无色和紫红色 | 氧化性:Br2>Fe3+>I2 |
D | 向浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1的AgNO3溶液,产生的沉淀呈黄色 | Ksp(AgCl)<Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:实验题
某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。实验过程如下:
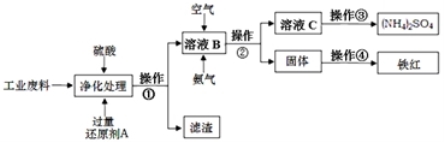
回答下列问题:
(1)滤渣的成分为 ,操作①的名称为 。
(2)上图溶液B中所发生反应的离子方程式为 。
(3)实验要求向溶液B中通入过量的空气,证明通入空气过量的方法是 。
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要 。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
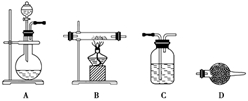
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→________→________→________→D(除D装置外,其它装置不能重复使用),最后D装置中所加药品为_______________,其作用是___________________。
②点燃B处酒精灯之前必须进行的操作是 。
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:选择题
化学与人类生产、生活、社会可持续发展密切相关。下列有关说法正确的是
A.MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al
B.水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质
C.高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2=2O3有单质参加,属于氧化还原反应
D.向水中加入明矾进行杀菌消毒
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
下列过程一定释放出能量的是:
A.化合反应 B.分解反应 C.原子组成分子 D.分子拆成原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com