
 B.
B. C.
C. D.
D.



科目:高中化学 来源:不详 题型:单选题
| A.分子个数:③>④>①=② | B.原子个数:③>④>①>② |
| C.体 积:③>④>①=② | D.质 量:③>①>④>② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
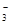 、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO
、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO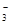 )︰n(SO42—)︰n(Fe3+)︰n(H
)︰n(SO42—)︰n(Fe3+)︰n(H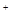 )︰n(M)=2︰3︰1︰3︰1,则M可能是下列中的
)︰n(M)=2︰3︰1︰3︰1,则M可能是下列中的| A.Fe2+ | B.Cu2+ | C.Al3+ | D.Ba2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2 NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
C.a g某气体含分子数为b,c g该气体在标况下的体积为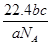 L L |
| D.某密闭容器盛有0.1 molN2和0.3 molH2,在一定条件下充分反应,转移电子的数目为0.6 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.在同温同压下,相同体积的任何气体单质所含的原子数目相同 |
| C.14 g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.含2molH2SO4的浓硫酸与足量铜片在加热条件下反应,一定能产生NA个SO2气体分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 砝码质量 | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 | 先↓后↑ | ↓ | 先↓后↑ | ↓ | 先↓后↑ |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下2.24 L H2O中,分子数为0.1NA |
| B.将1mol Cl2通入到水中,则N(HClO)+ N(Cl?)+ N(ClO-)= 2NA |
| C.常温常压下16g O2和O3混合气体中,氧原子数为NA |
| D.7.8g Na2O2与足量水反应,转移电子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com