
工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3。Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用。某科研小组用该原理处理污水,设计的装置如图所示。下列说法正确的是 ( )。
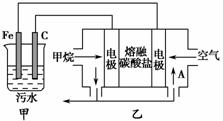
A.为了增加污水的导电能力,应向污水中加入适量的H2SO4溶液
B.甲装置中Fe电极的反应为Fe-3e-===Fe3+
C.为了使燃料电池乙长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2
D.当乙装置中有1.6 g CH4参加反应时,C电极理论上生成气体的体积在标准状况下为4.48 L
科目:高中化学 来源: 题型:
高温及催化剂作用下,某反应的平衡常数K= 。恒容时,温度升高,H2浓度减小,下列说法正确的是 ( )。
。恒容时,温度升高,H2浓度减小,下列说法正确的是 ( )。
A.恒温下,将容器体积变为原来2倍,CO的平衡浓度变为原来的1/2
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,正反应速率减小,逆反应速率增大
D.该反应化学方程式为CO2+H2 CO+H2O ΔH<0
CO+H2O ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
已知 H2SO4(aq)与 Ba (OH)2(aq)反应的 ΔH=-1 584.2 kJ·mol-1;HCl (aq) 与NaOH (aq) 反应的 ΔH=-55.6 kJ·mol-1。则生成 BaSO4 (s) 的反应热等于 ( )。
A.-1 528.6 kJ·mol-1 B.-1 473 kJ·mol-1
C.+1 473 kJ·mol-1 D.+1 528.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
为节省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、CuSO4 溶液、直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器(用品),通过巧妙的构思,设计了比较铜、锌金属活动性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),向烧杯中小心加入稀硫酸,观察到的现象是
________________________________________________________________。
甲同学的设计思路是______________________________________________。
(2)乙同学接着甲的实验,向烧杯中滴加________溶液,进而观察到的现象是______________________________________________________________。
乙同学作出锌、铜金属活动性相对强弱的结论所依据的原理是________________________________________________________________________。
(3)丙同学使用直流电源、石墨电极组装好电解装置,向乙同学实验后的溶液中补充了必要的试剂________溶液(作为电解液)。反应在调控下随即开始,实验中有关反应的化学方程式为______________________________________。
实验中的明显现象是______________________________________________。
(4)请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌、铜金属活动性的相对强弱(简要说明操作和现象)___________________________________________________________
_______________________________________________________________
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
近日,中美联合研究小组通过共同努力,采用廉价的钠离子,同时使用纳米氧化锰和锂材料作电极制造出了钠离子充电电池,其工作原理示意图如图所示。关于该电池的说法中正确的是 ( )。
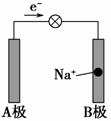
A.放电时A极作正极
B.放电时Na+ 向负极移动
C.充电时是将化学能转化为电能
D.充电时B极为阳极,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法错误的是
A.一定条件下,2molSO2和1molO2混合在密闭容器中
充分反应后容器中的分子数大于2NA
B.256g S8分子中含S-S键为7NA个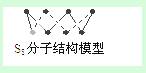
C.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个
D.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素的化合物应用十分广泛。请回答:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,则该反应的热化学方程式为 。

(2)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
①298k时,该反应的平衡常数为 L·mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变; B.混合气体的颜色不再变化; C.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)=0.6 moln(N2O4)=1.2mol,则此时V(正) V(逆)(填 “>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点。
①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序 。
③d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在可逆反应中,平衡常数与反应进行的限度的关系正确的是( )
A.K越大,反应程度越大
B.K越大,反应程度越小
C.K的大小与反应程度无关
D.升高温度,K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一。下列对有关实验事实的解释正确的是( )
A.SO2气体使高锰酸钾溶液褪色,表现了SO2的漂白性
B.在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是Cu
C.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
D.常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com