
(1)分析下列物质的物理性质,判断其晶体类型。
A.碳化铝,黄色晶体,熔点2200 ℃,熔融态不导电________;
B.溴化铝,无色晶体,熔点98 ℃,熔融态不导电________;
C.五氟化钒,无色晶体,熔点19.5 ℃,易溶于乙醇、氯仿、丙酮中________;
D.溴化钾,无色晶体,熔融时或溶于水中都能导电________。
(2)三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为________。
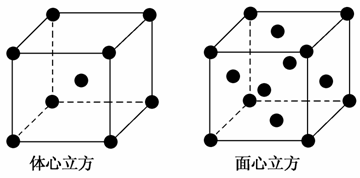
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如上图所示。面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为________。
解析 (1)晶体的熔点高低、熔融态能否导电及溶解性等性质相结合,是判断晶体类型的重要依据。原子晶体和离子晶体的熔点都很高或较高,两者最大的差异是熔融态的导电性不同。原子晶体熔融态不导电,离子晶体熔融时或水溶液都能导电。原子晶体和分子晶体的区别则主要在于熔、沸点有很大差异。一般原子晶体和分子晶体熔融态时都不能导电。另外易溶于一些有机溶剂的物质往往也是分子晶体的特征之一。
(2)根据题给信息,FeCl3的熔沸点低,易溶于水、有机溶剂等,可确定其为分子晶体。
(3)面心立方中铁原子个数为8×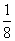 +6×
+6×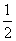 =4,体心立方中铁原子个数为8×
=4,体心立方中铁原子个数为8×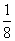 +1=2个,两晶胞中实际含有的铁原子的个数比为2:1。
+1=2个,两晶胞中实际含有的铁原子的个数比为2:1。
答案 (1)原子晶体 分子晶体 分子晶体 离子晶体
(2)分子晶体
(3)2:1


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列各组离子能大量共存的是
①“84”消毒液的水溶液中:Fe2+、Cl—、Ca2+、Na+
②加入KSCN显红色的溶液:K+、N 、Cl—、S2—
、Cl—、S2—
③能够与金属Cu常温下反应放出气体的溶液;Fe3+、Al3+、S 、K+
、K+
④pH=2的溶液中:N 、Na+、Cl—、Cu2+
、Na+、Cl—、Cu2+
⑤无色溶液中:K+、CH3COO—、HC 、Mn
、Mn
A.②③ B.①③ C.①⑤ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质的晶体中,含A 、B
、B 、C
、C 三种元素,其排列方式如图所示(其中前后两面心上的B原子未画出)。晶体中的A、B、C的原子个数比依次为( )
三种元素,其排列方式如图所示(其中前后两面心上的B原子未画出)。晶体中的A、B、C的原子个数比依次为( )

A.1:3:1 B.2:3:1
C.2:2:1 D.1:3:3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质类别判断的依据正确的是( )
A.原子晶体:晶体的熔点是否很高
B.电解质:水溶液是否导电
C.离子化合物:是否含有离子键
D.共价化合物:是否含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质各自形成晶体,均属于分子晶体的化合物是( )
A.NH3、HD、C10H8 B.PCl3、CO2、H2SO4
C.SO2、SiO2、P2O5 D.CCl4、Na2S、H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2原子晶体的说法正确的是( )
A.CO2原子晶体和分子晶体互为同素异形体
B.在一定条件下,CO2原子晶体转化为分子晶体是物理变化
C.CO2原子晶体和CO2分子晶体具有相同的物理性质
D.在CO2原子晶体中,每一个碳原子周围结合四个氧原子,每个氧原子跟两个碳原子相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
在盐的水解过程中,下列叙述正确的是( )
A.盐的电离平衡被破坏
B.水的电离平衡被破坏
C.含有弱酸根离子的盐的水溶液一定显碱性
D.盐的水解程度主要取决于盐本身的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
把一定量的Na2O2和NaHCO3的混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为2.24L(标况);再将此气体通入另一份混合物中,恰好完全反应后,得到O2 2.016L(标况),则加入稀盐酸的物质的量浓度是( )
|
| A. | 3.4mol/L | B. | 0.2mol/L | C. | 1.8mol/L | D. | 3.6mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com