
| A、0.01 mol/L的蔗糖溶液 |
| B、0.01 mol/L的K2SO4溶液 |
| C、0.02 mol/L的NaCl溶液 |
| D、0.02 mol/L的CH3COOH溶液 |


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
| A、全部 | B、①④ | C、①③ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na在足量O2中燃烧,消耗l mol O2时转移的电子数是4×6.02×1023 |
| B、盐酸和醋酸的混合溶液pH=1,该溶液中c(H+)=0.1 mol/L |
| C、1 L 0.1 mol/L NH4Cl溶液中的NH4+数是0.1×6.02×1023 |
| D、标准状况下2.24 L Cl2中含有0.2 mol 共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA |
| B、0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA |
| C、反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol放出热量9.2 kJ时,转移电子0.6 NA |
| D、0.1 mol H2O2分子中含极性共价键数目为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2 |
| B、CO2 |
| C、NH3 |
| D、SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
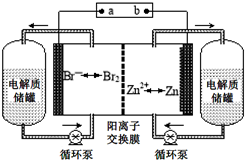 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是( )| A、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| B、放电时负极的电极反应式为Zn-2e-=Zn2+ |
| C、充电时电极a连接电源的负极 |
| D、放电时左侧电解质储罐中的离子总浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com