
【题目】Ⅰ.SF6是一种优良的绝缘气体,分子结构中,只存在S—F键,已知1 mol S(s)转化为气态硫原子吸收能量280 kJ,F—F键能为160 kJ·mol-1,S—F键能为330 kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式_______________________________。
Ⅱ.V、W、X、Y、Z是由四种短周期元素中的2种或3种组成的5种化合物,其中W、X、Z均由2种元素组成,X是导致温室效应的主要气体,Z是天然气的主要成分,Y、W都既能与酸反应,又能与强碱溶液反应。上述5种化合物涉及的四种元素的原子序数之和等于28;V由一种金属元素A和两种非金属元素B与C组成,其化学式构成为A(BC3)3 。它们之间的反应关系如下图:

(1)写出物质W的一种用途:__________________________________________________。
(2)写出V与足量NaOH溶液反应的化学方程式:________________________________。
(3)将少量的X通入某种物质的水溶液中可以生成Y,该反应的离子方程式为________________________________________________________________________。
(4)写出气体X的结构式__________。
(5)以Z为燃料,活性炭为电极,熔融碳酸盐(如熔融K2CO3)环境下制成燃料电池的负极反应式为_________________________________________________。
【答案】 S(s)+3F2(g)===SF6(g) ΔH=-1 220 kJ·mol-1 作高温耐火材料或冶炼金属铝 Al(CH3)3+NaOH+H2O===NaAlO2+3CH4↑ CO2+2AlO![]() +3H2O===2Al(OH)3↓+CO32─
+3H2O===2Al(OH)3↓+CO32─ ![]() CH4+4CO
CH4+4CO![]() -8e-===5CO2+2H2O
-8e-===5CO2+2H2O
【解析】Ⅰ.反应热△H=反应物总键能-生成物总键能,所以对于S(s)+3F2(g)═SF6(g),其反应热△H=280KJ/mol+3×160KJ/mol-6×330KJ/mol=-1220kJ/mol,热化学方程式为:S(s)+3F2(g)===SF6(g) ΔH=-1 220 kJ·mol-1。
Ⅱ.X是导致温室效应的主要气体,应为CO2,Z是天然气的主要成分,应为CH4,Y、W都既能与酸反应,又能与强碱溶液反应,应为两性化合物,由转化关系可知Y为Al(OH)3,W为Al2O3,则V中含有C、Al、H元素,原子个数比为1:3:9,应为Al(CH3)3。(1)物质W为氧化铝可应用于作高温耐火材料或冶炼金属铝;(2)V[Al(CH3)3]与足量NaOH溶液反应的化学方程式:Al(CH3)3+NaOH+H2O===NaAlO2+3CH4↑。(3)将少量的X(CO2)通入某种物质的水溶液中可以生成Y[Al(OH)3],反应的离子方程式为:CO2+2AlO![]() +3H2O===2Al(OH)3↓+CO32─;(4)写出气体X(CO2)的结构式为
+3H2O===2Al(OH)3↓+CO32─;(4)写出气体X(CO2)的结构式为![]() ;(5) Z(CH4)在活性炭电极上失去电子,与碳酸根离子结合生成二氧化碳,电池的负极反应式为CH4+4CO
;(5) Z(CH4)在活性炭电极上失去电子,与碳酸根离子结合生成二氧化碳,电池的负极反应式为CH4+4CO![]() -8e-===5CO2+2H2O。
-8e-===5CO2+2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】【化学选修5:有机化学基础】芳香族化合物A是一种降血脂药物,A不能与Na反应。其合成路线如下:

已知:
I.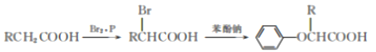
II.RCH==CH2![]() RCH2CH2Br
RCH2CH2Br
III.烃C的核磁共振氢谱只有两组峰,它的质谱图如图所示:

IV.K的结构具有对称性:I能发生银镜反应且1molI能与2molH2发生加成反应。试回答下列问题:
(1)烃C的化学名称为_______________________。
(2)H分子中含有的官能团名称为_____________;反应的条件为____________________。
(3)写出J与新制银氨溶液发生反应的化学方程式:______________________________________。
(4)反应④的化学方程式为:____________________________________________。
(5)符合下列3个条件的H的同分异构体有____种,其中氢原子共有五种不同环境的是(写结构简式)__________________________________________。
①能与FeCl溶液显色;②苯环上只有2个取代基;③1mol该物质最多可消耗1molNaHCO3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①CH3OH(g)+![]() O2(g)===CO2(g)+2H2O(g) ΔH1=-a kJ·mol-1
O2(g)===CO2(g)+2H2O(g) ΔH1=-a kJ·mol-1
②CO(g)+![]() O2(g)===CO2(g) ΔH2=-b kJ·mol-1
O2(g)===CO2(g) ΔH2=-b kJ·mol-1
③H2(g)+![]() O2(g)===H2O(g) ΔH3=-c kJ·mol-1
O2(g)===H2O(g) ΔH3=-c kJ·mol-1
④H2(g)+![]() O2(g)===H2O(l) ΔH4=-d kJ·mol-1 下列叙述正确的是
O2(g)===H2O(l) ΔH4=-d kJ·mol-1 下列叙述正确的是
A. 由上述热化学方程式可知ΔH3<ΔH4
B. H2的燃烧热为d kJ·mol-1
C. CH3OH(g)===CO(g)+2H2(g) ΔH=( a- b-2c)kJ·mol-1
D. 当CO和H2的物质的量之比为1∶2时,其完全燃烧生成CO2和H2O(l)时,放出Q kJ热量,则混合气中CO的物质的量为![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-═IO3-+5I-+3H2O下列说法不正确的是( )
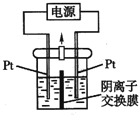
A. 右侧发生的电极方程式:2H2O+2e-═H2↑+2OH-
B. 电解结束时,右侧溶液中含有IO3-
C. 电解槽内发生反应的总化学方程式:![]()
D. 如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总反应不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用饱和氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
A.将饱和氯化铁溶液滴入蒸馏水中即可
B.将饱和氯化铁溶液滴入热水中,至溶液呈深黄色
C.将饱和氯化铁溶液滴入沸水中,继续煮沸至溶液呈红褐色
D.将饱和氯化铁溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在唾液淀粉酶催化淀粉分解实验中,将唾液稀释10倍,与用唾液原液(没稀释)实验效果基本相同,这表明酶具有
A.专一性 B.稳定性
C.多样性 D.高效性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列说法正确的是( )
A.1 mol NO中含有的原子数目为2NA
B.常温下,22.4L氮气含有的原子数目为2NA
C.1L1 mol L﹣1 MgS04溶液中含有的Mg2+数目为2NA
D.2.8 g硅单质与足量氧气在高温下完全反应时,硅原子失去的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图甲装置进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是( )
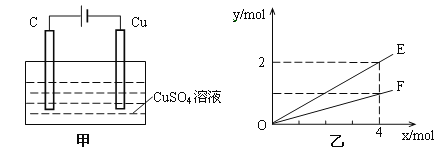
A. E表示生成铜的物质的量
B. E表示反应消耗水的物质的量
C. F表示反应生成氧气的物质的量
D. F表示生成硫酸的物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com