


科目:高中化学 来源: 题型:
| A、在常温常压下,11.2L氮气含有的分子数为0.5NA |
| B、在标准状况下,22.4L水的质量约为18g |
| C、32g氧气所含的原子数为2NA |
| D、相同质量的磷酸和硫酸所含的原子数目相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上粗铜的电解精炼时,每转移1mol电子时阳极上溶解的铜小于0.5NA |
| B、将1mol NO2气体在降温后颜色变浅,但其所含的分子数仍然为NA |
| C、1mol NaHSO4固体中含阴阳离子数为3NA |
| D、1.12L Cl2含有1.7NA个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化反应与还原反应一定同时发生,但氧化剂、还原剂可不直接接触,且氧化产物与还原产物在任何条件下不可能发生反应 |
| B、工业制硫酸、工业制硝酸、由石英获取单晶硅全程变化均为氧化还原反应 |
| C、氮化镁、硫化铝、碳化钙、氢化钠与水反应,水既不做氧化剂也不做还原剂 |
| D、用惰性电极电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672 mL(标准状况下)时,溶液的pH为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9.6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
| A、①中溶解了5.6gFe |
| B、硝酸的浓度为4mol/L |
| C、②中溶解了9.6gCu |
| D、④中V=7840 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 可再生能源是我国重要的能源资源,在能源要求、改善能源结构、减少环境污染、促进经济发展等方面具有重要作用.应用太阳能光伏发电技术是实现节能减排的一项重要措施.下列有关分析不正确的是( )
可再生能源是我国重要的能源资源,在能源要求、改善能源结构、减少环境污染、促进经济发展等方面具有重要作用.应用太阳能光伏发电技术是实现节能减排的一项重要措施.下列有关分析不正确的是( )| A、风能、太阳能、生物质能等属于可再生能源 |
| B、推广可再生能源有利于经济可持续发展 |
| C、如图是太阳能光伏发电原理图,图中A极为正极 |
| D、光伏发电能量转化方式是太阳能直接转变为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
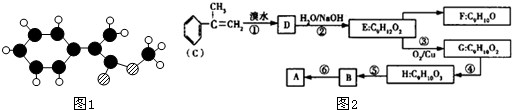
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温常压下,11.2LN2含有的分子数为0.5NA |
| B、在常温常压下,1molH2含有的原子数为NA |
| C、71gCl2所含原子数为2 NA |
| D、23g钠所具有的电子数目为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2011年4月10日,我国在西昌卫星发射中心用“长征三号甲”运载火箭,成功将第八颗北斗导航卫星送入太空预定转移轨道.该火箭所用燃料是偏二甲肼(CH3-NH-NH-CH3)和四氧化二氮(N2O4).在火箭升空过程中,燃料发生反应:CH3-NH-NH-CH3+2N2O4→2CO2+3N2+4H2O,提供能量.下列有关叙述正确的是( )
2011年4月10日,我国在西昌卫星发射中心用“长征三号甲”运载火箭,成功将第八颗北斗导航卫星送入太空预定转移轨道.该火箭所用燃料是偏二甲肼(CH3-NH-NH-CH3)和四氧化二氮(N2O4).在火箭升空过程中,燃料发生反应:CH3-NH-NH-CH3+2N2O4→2CO2+3N2+4H2O,提供能量.下列有关叙述正确的是( )| A、该反应中N2O4是氧化剂,偏二甲肼是还原剂 |
| B、N2是氧化产物,CO2是还原产物 |
| C、CO2是氧化产物,N2是还原产物 |
| D、每有0.6molN2生成,转移电子数目为2.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com