
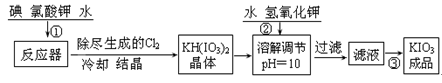
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液。 | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡。 | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡。 | 溶液变蓝色 |
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源:不详 题型:填空题
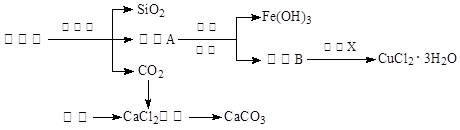
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
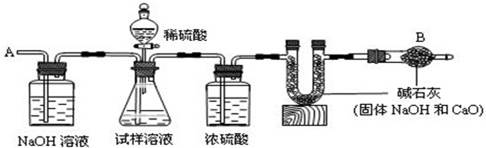
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
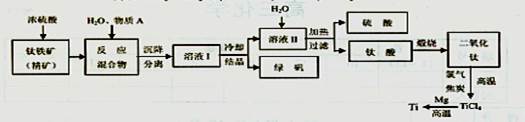
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
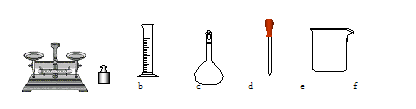
| A.称取8.0g胆矾,在480mL /c中定容 |
| B.称取12.5g胆矾,在500mL /e中定容 |
| C.称取8.0g硫酸铜,在500mL /c中定容 |
| D.称取12.50g胆矾,在500mL /c中定容 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
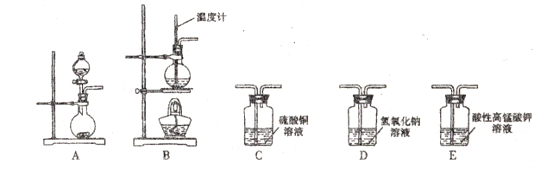
| 序号 | 气体 | 装置连接顺序(填字母) | 制作反应的化学方程式 |
| (1) | 乙烯 | _____________________ | ______________ |
| (2) | 乙炔 | A→C→E | ___________ |
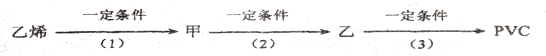
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
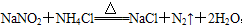 ,关于该反应的说法正确的是( )
,关于该反应的说法正确的是( )| A.生成1 molN2时转移的电子为6 mol | B.NaNO2是氧化剂 |
| C.NH4Cl中的N元素被还原 | D.N2既是氧化剂又是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com