
下列说法正确的是
A.CO(g)的燃烧热:ΔH=-283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的
ΔH=+566.0kJ/mol
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3 kJ·mol-1,
则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
C.己知2C(s)+2O2(g)=2CO2(g) △H = a;2C(s)+O2(g)=2CO(g);△H = b,则a>b
D.已知C (石墨,s)=C (金刚石,s) △H>0,则石墨比金刚石稳定
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式 ;
②SiO2晶体的空间构型及硅氧之间的成键方式 ;
③已知SnO2是离子晶体,写出其主要物理性质 (写出2条即可)
CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为
(4)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度 (填字母)
A 强 B 弱 C 相等 D 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想,其中不成立的是
A.Mg(NO3)2、NO2、O2 B.MgO、NO2、O2
C.Mg3N2、O2 D.MgO、NO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
对于给定的可逆反应的平衡常数(K)的说法正确的是
A.K只与温度有关,温度不变,K不变
B.改变条件,反应物的转化率增大,K也一定增大
C.温度一定时,其正、逆反应的K相等
D.若正反应ΔH<0,升高温度,该反应的K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.室温下,将pH=2的醋酸与pH=12的NaOH溶液等体积混合,溶液显中性
B.室温下,向pH=3的醋酸溶液加水稀释后,溶液中所有离子浓度均减小
C.向含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
D.向CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
(a)铁元素在人类生活中扮演着非常重要的角色,不仅仅是重要的建筑材料,
也是人体必须的微量元素。每年钢铁的腐蚀带来巨大的经济损失。某校研究小组在实验室中模拟钢铁在自然环境下的腐蚀,设置如下装置,几天后观察结果:
请回答下列问题:
(1)请比较以上三个装置中右侧导管中红墨水的高度:____>____>____。
请写出A装置中,钢铁锈蚀时正极反应的电极反应式_____________________。
(2)钢铁的防腐有重大的意义,生活中常将金属制品放在干燥处或者涂上矿物油予以保
护,现请你从电化学角度设计一种方法保护下图中钢铁以免被腐蚀,请将下图完成:
 |
(b)下面是一种常见补铁药品说明书中的部分内容:该药品含Fe2+ :33%~36%,不
溶于水但能溶于人体中的胃酸,与Vc(维生素C)同服可增加本品吸收。某乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为:

准确称量上述药品10.00g,将其全部溶于试剂1中,配制成1000mL溶液,取
出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(3)该实验中的试剂1是______(填序号)。
A.蒸馏水 B.稀盐酸 C.稀硫酸 D.稀硝酸
(4)请简述判断滴定终点的现象:___________________________________________。
(5)请通过计算,说明该药品含“铁”量是否合格____________(填“合格”或“不合格”)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中书写正确的一组是
① 向明矾溶液中加入Ba(OH)2溶液至A13+ 刚好完全沉淀:
Al3++ SO42-+3OH-+Ba2+= BaSO4↓+Al (OH)3↓
② 氟气和水反应:2F2+2H2O = 4H++4F-+O2
③ 向澄清石灰水中加入少量小苏打溶液:
Ca2++OH-+HCO3- = CaCO3↓+H2O
④ 铜片投入稀HNO3溶液:Cu+NO3-+4H+ = NO↑+2H2O+Cu2+
⑤ 钠与水反应:Na +2 H2O = Na+ +OH— + H2↑
|
⑦ 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O==Fe(OH)3(胶体)+3H+
⑧ 过量氯水与FeI2溶液作用: 2Fe2+ + 2I—+ 2Cl2 = 2 Fe3+ + I2 + 4Cl—
A. ①②③④ B. ③⑦ C. ①③④⑤ D.①④⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
2.3 g纯净金属钠在干燥空气中被氧化后得到3.5 g固体,由此可判断其氧化物是
A.只有Na2O B.只有Na2O2 C.Na2O和Na2O2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )
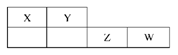 A.氢化物稳定性:X>Y
A.氢化物稳定性:X>Y
B.最高价氧化物对应的水化物的酸性:W>Y
C.4种元素的单质中,W单质的熔、沸点最高
D.干燥的W单质具有漂白性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com