
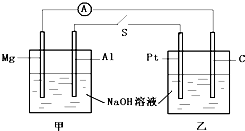
 如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )| A、电流计指针不发生偏转 |
| B、Al、Pt两电极有氢气生成 |
| C、Mg、C两电极生成的气体在一定条件下可以恰好完全反应 |
| D、甲池pH减小,乙池pH不变 |


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
 有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示.已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题:
有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示.已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅和氯化镁熔化 |
| B、碘和氯化铵受热变成气体 |
| C、钠和硫受热变成气体 |
| D、氯化钠和硝酸钠溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤正确 | B、都不正确 |
| C、③④正确 | D、仅⑤正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、原硫酸铜溶液的密度为ρ=
| ||
B、原硫酸铜溶液的物质的量浓度为c(CuSO4)=
| ||
C、原硫酸铜溶液的质量分数ω(CuSO4)=
| ||
D、生成硫酸铜晶体的物质的量为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、18g水含有电子数为8NA |
| C、标准状况下,22.4L氢气含有氢原子个数为2NA |
| D、22.4L氢气一定含有NA 个氢分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com