
向NaBr、NaI、Na2CO3的混合溶液中通入足量氯气后,将溶液蒸于并充分灼烧,得到固体剩余物的组成可能是
A.NaCl B.NaCl、NaHCO3
C.NaCl、I2 D.NaCl、NaI、Na2CO3
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
下列说法正确的( )
A、燃料电池由外设装备提供燃料和氧化剂
B、Mg和Al通常用热还原的方法来冶炼
C、绿色化学的核心是应用化学原理对环境污染进行治理
D、蛋白质、棉花、淀粉、油脂都是由高分子组成的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。
已知: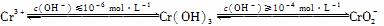
(1) 在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
① 写出Cr2O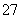 与FeSO4溶液在酸性条件下反应的离子方程式:________________。
与FeSO4溶液在酸性条件下反应的离子方程式:________________。
② 用离子方程式表示溶液pH不能超过10的原因:____。
(2) 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O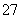 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
① 写出阴极的电极反应式:________________。
② 电解法中加入氯化钠的作用是________________。
(3) 铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
① CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为____。
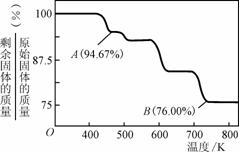
② CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如右图所示,则B点时剩余固体的成分是________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式表达正确的是
A.鸡蛋壳浸泡在盐酸中产生气泡: +2H+
+2H+
 CO2+H2O
CO2+H2O
B.四氧化三铁固体溶解在稀硝酸溶液中:Fe3O4+8H+ 2Fe3++Fe2++4H2O
2Fe3++Fe2++4H2O
C.将氨气通入硫酸溶液中:NH3+H+
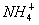
D.向碳酸氢铵溶液中加入足量的NaOH溶液: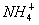 +OH-
+OH- NH3·H2O
NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、铝、铜及其化合物在生产、生活中有广泛的用途。试回答下列问题:
(1)铝的原子结构示意图为________;铁、铝、铜三种金属的金属活动性由弱到强的排列顺序是________________。
(2)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,请写出该反应的离子方程式:________________________。
(3)如图K82所示的装置中,铁作________极,铜电极的电极反应式为________________。
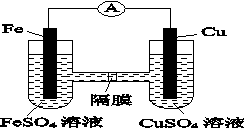
图K82
(4)已知铜与稀硫酸不反应,但铜片在稀硫酸中长时间加热时溶液会呈蓝色,请用化学方程式表示其原因:________________________________。
(5)氯化铝广泛用作有机合成和石油工业的催化剂。将铝土矿粉(主要成分为Al2O3)与焦炭混合后加热,并通入氯气,可得到氯化铝,同时生成CO。写出该反应的化学方程式:________________________________________。该反应中的氧化剂是________。
(6)某校兴趣小组为测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46 g该合金粉末,加入过量盐酸,充分反应后过滤,测得剩余固体的质量为0.07 g。向滤液中滴加足量NaOH浓溶液,充分搅拌、过滤、洗涤得到固体。再将所得固体充分加热、灼烧,得到红棕色粉末1.60 g。通过计算确定此合金的组成为____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.酸式盐的水溶液一定显酸性 B.酸性氧化物一定是非金属氧化物
C.丁达尔效应是溶液和胶体的本质区别 D.HClO是弱酸,但NaClO是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形。Q的各级电离能如下表,W与R是同族元素。
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
回答下列有关问题:
(1)W形成单质的晶体类型是_____________;其单核离子结构示意图为_____________。
(2)化合物Q2W2的电子式__________,化合物XYZ的结构式________________。
(3)Y与X形成式量最小,且分子中含有非极性键的分子式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
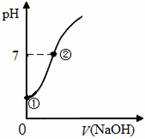
常温下,向饱和氯水中逐滴滴入0.1mol·L-1的氢氧化钠溶液,pH变化如下图所示,下列有关叙述正确的是
A.①点所示溶液中只存在HClO的电离平衡
B.②点所示溶液中:c(Na+)=c(Cl-) + c(ClO-)
C.I-能在②点所示溶液中存在
D.①到②水的电离程度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:
CO2(g)+H2(g)  CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数K2=________,反应
CO2(g)+H2(g)的平衡常数K2=________,反应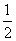 CO2(g)+
CO2(g)+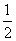 H2(g)
H2(g) 
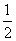 CO(g)+
CO(g)+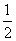 H2O(g)的平衡常数K3=________。
H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正________v逆(填“>”、“=”或“<”)。该温度下反应达到平衡时,CO2的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com