
下列有关实验现象的预测或装置的选用正确的是
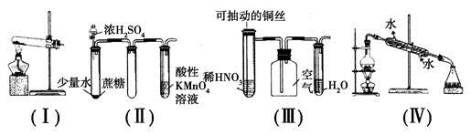
A.用装置(Ⅰ)加热草酸晶体获取某些气体(草酸晶体的熔点101.5 ℃,分解温度约为150 ℃)
B.用装置(Ⅱ)进行实验时,酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C.用装置(Ⅲ)进行实验时,广口瓶内先有浅红棕色气体出现后又变为无色,且不会产生空气污染
D.用装置(Ⅳ)分离溴苯和苯的混合物
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源:2014高考名师推荐化学--预测2 题型:选择题
化学与生活密切相关;下列说法不正确的是
A.PM2.5也称细颗粒物,对空气质量和能见度等有重要的影响
B.稀豆浆、硅酸、氯化铁溶液、空气均为胶体
C.聚乙烯塑料制品可用于食品的包装
D.次氯酸钠溶液可用于环境的消毒杀菌
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测16 题型:选择题
下列离子方程式书写正确的是
A.硫酸铝溶液中滴加过量浓氨水:Al3++4NH3·H2O===AlO2-+4NH4+ +2H2O
B.乙酸钠溶液显碱性的原因:CH3COO-+H2O===CH3COOH+OH-
C.氢氧化钠溶液吸收少量SO2气体:SO2+2OH-===SO32- +H2O
D.漂白粉放置在空气中变质:ClO-+CO2+H2O===HClO+HCO3-
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
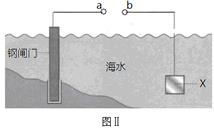
图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法不正确的是
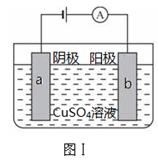
A、图Ⅰ中a为纯铜
B、图Ⅰ中SO42-向b极移动
C、图Ⅱ中如果a、b间连接电源,则a连接负极
D、图Ⅱ中如果a、b间用导线连接,则X可以是铜
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
某温度下,将溶质质量分数为a%的KOH溶液蒸发掉m g水后恢复至原温度,恰好得到质量分数为2a%的KOH饱和溶液V mL,则下列说法中正确的是
A.该温度下KOH的溶解度为100a/(100-a)g
B.原溶液的质量为2m g
C.可以求算原溶液的物质的量浓度
D.保持温度不变,向原溶液中加入2a g KOH可达饱和
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌。“一滴香”的分子结构如图所示,下列说法正确的是
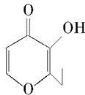
A.该有机物的分子式为C7H7O3
B.该有机物能发生取代、加成和氧化反应
C.1 mol该有机物最多能与2 mol H2发生加成反应
D.该有机物的一种芳香族同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:选择题
下列条件下,离子能大量共存或者离子方程式正确的是( )
A、pH=1的溶液中:Fe2+、ClO-、Na+、SO42-
B、在含较多Al3+的溶液中:K+、Cl-、HCO3-
C、一小块钠投入到CuSO4溶液中:2Na+Cu2+= Cu+2Na+
D、铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2++ 2NO↑+ 4H2O
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测13 题型:实验题
如图所示是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。

(1)在组装好装置后,若要检验A—E装置的气密性,其操作是首先 ,然后微热A,???察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成说明装置气密性良好。
(2)装置B中盛放试剂是 。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹1,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,稍后片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时产生 (答现象);从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式 。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量。若反应前固体质量为16g,反应后称重固体质量减少2.4g。通过计算确定该固体产物的成分是 (用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。写出产生白烟的化学方程式 。迅速产生倒吸的原因是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:简答题
含硫化合物在工业生产中有广泛的用途。
(1)SO2可用于工业生产SO3。
①在一定条件下,每生成8g SO3气体,放热9.83kJ。该反应的热化学方程式为________。
②在500℃,催化剂存在的条件下,向容积为1L的甲、乙两个密闭容器中均充入 2 mol SO2和1 mol O2。甲保持压强不变,乙保持容积不变,充分反应后均达到平衡。
I.平衡时,两容器中SO3体积分数的关系为:甲_______乙(填“>”、“<”或“ =”)。
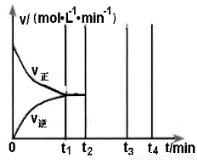
II.若乙在t1 min时达到平衡,此时测得容器乙中SO2的转化率为90%,则该
反应的平衡常数为_______;保持温度不变,t2 min时再向该容器中充入1 mol SO2和1 mol SO3,t3min时达到新平衡。请在下图中画出t2~t4 min内正逆反应速率的变化曲线(曲线上必须标明V正、V逆 )
(2)硫酸镁晶体(MgSO4·7H2O )在制革、医药等领域均有广泛用途。4.92g硫酸镁晶体受热脱水过程的热重曲线(固体质量随温度变化的曲线)如右图所示。
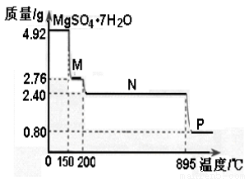
①固体M的化学式为__________。
②硫酸镁晶体受热失去结晶水的过程分为_________个阶段。
③N转化成P时,同时生成另一种氧化物,该反应的化学方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com