

| A�� | �ݢۢ� | B�� | �ڢۢ� | C�� | �ۢݢ� | D�� | �ۢڢ� |
���� �����ʵ���Ũ�ȡ��������MgCl2��BeCl2��AlCl3��Һ�������ߵ����ʵ�������ȵģ���һ��Ũ�ȵ�NaOH��Һ���ֱ����������Һ�����������������ķ�Ӧ�������£�MgCl2+2NaOH=Mg��OH��2��+2NaCl��BeCl2+2NaOH=Be��OH��2��+2NaCl��Be��OH��2��+2NaOH=Na2BeO2+2H2O��AlCl3+3NaOH=Al��OH��3��+3NaCl��Al��OH��3��+NaOH=NaAlO2+2H2O��������Һ���ʵ����ͻ�ѧ����ʽ��ȷ������������
��� �⣺���Ȼ�þ�м����������ƣ���ʼ���к����е��������ᣬȻ�����ɰ�ɫ����������þ�����������ƹ���ʱ������Ҳ�����ܽ⣬�����ֲ��䣬�ʶ�Ӧ����ͼ��ۣ�
���Ȼ�����Һ�м����������ƣ���ʼ���к����е��������ᣬȻ�����ɰ�ɫ����������п�����������ƹ���ʱ���������ܽ⣬���η�����ӦBeCl2+2NaOH=Be��OH��2��+2NaCl��Be��OH��2��+2NaOH=Na2BeO2+2H2O���������ﵽ���ͳ�����ȫ��ʧ�����ĵ�������������ȵģ���ͼ�������ȷ�ģ�
���Ȼ�����Һ�м����������ƣ���ʼ���к����е��������ᣬȻ�����ɰ�ɫ�����������������������ƹ���ʱ���������ܽ⣬���η�����Ӧ��
AlCl3+3NaOH=Al��OH��3��+3NaCl��Al��OH��3��+NaOH=NaAlO2+2H2O���������ﵽ���ͳ�����ȫ��ʧ�����ĵ��������Ƶ����ʵ���֮����3��1����ͼ�������ȷ�ģ�����BeCl2��MgCl2��AlCl3������Һ��Ӧ��ͼ����ȷ���Ǣݢۢ٣���A��ȷ��
��ѡA��
���� ���⿼���˽���þ���������Լ�������Ŀ���������Һ��ǿ����������֮��ķ�Ӧ�����ڻ�ѧ��Ӧ֪ʶ�Ŀ����⣬ע�ⷽ��ʽ�����Ӧ���ǽ���ؼ�����Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͼ���������


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
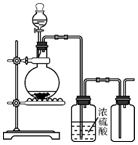
| A�� | ͭ��ϡ������һ������ | B�� | ���������������ƶ������� | ||
| C�� | п��ϡ���������� | D�� | ��������ϡ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
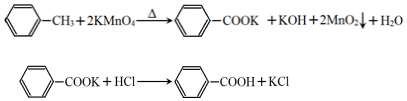
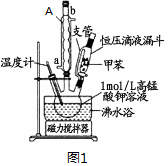
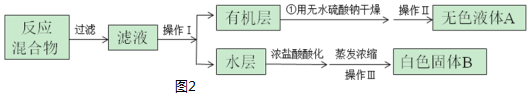
| ��һ�� | �ڶ��� | ������ | ���Ĵ� | |
| �����mL�� | 24.00 | 24.10 | 22.40 | 23.90 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ϊ32g | B�� | ����ԭ����ΪNA | ||
| C�� | ����������ΪNA | D�� | �ڱ�״���£����ԼΪ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ���������������Ũ��Ϊ10-13 mol•L-1����Һ�У�Ca2+��K+��Cl-��HCO3-���������ܴ������� | |
| B�� | ��֪MgCO3��Ksp=6.82��10-6�������к��й���MgCO3����Һ�У�����c��Mg2+��=c��CO32-������c��Mg2+��?c��CO32-��=6.82��10-6 | |
| C�� | �����£���0.2 mol?L-1ijһԪ�ROH����Һ��0.1 mol?L-1HCl��Һ�������ϣ���Ϻ���ҺpH��7����c��ROH����c��R+�� | |
| D�� | ���ڷ�ӦN2H4��l��=N2��g��+2H2��g������H=-50.6 kJ?mol-1����ֻ�ڸ������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��״���£�22.4 L H2���е�ԭ������2NA | |
| B�� | ��״���£�NA��ˮ���ӵ������22.4 L | |
| C�� | �κ�����£�1 mol CO�ж�����NA������ | |
| D�� | ͨ��״���£�NA��NH3���ӵ������22.4 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=11����Һ | B�� | 4 g NaOH����ˮ�γ�1L��ˮ��Һ | ||
| C�� | c��OH-��=0.12 mol•L-1 | D�� | c��H+��=1��10-10 mol•L-1����Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com