
| A. | 283kJ•mol-1 | B. | +172.5 kJ•mol-1 | C. | -172.5 kJ•mol-1 | D. | -504 kJ•mol-1 |
分析 ①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
②C(s)+O2 (g)═CO2(g)△H2=-393.5kJ/mol
结合盖斯定律可知,①×2-②得到 C(s)+CO2(g)=2CO(g),以此来解答.
解答 解:①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
②C(s)+O2 (g)═CO2(g)△H2=-393.5kJ/mol
由盖斯定律可知,①×2-②得到 C(s)+CO2(g)=2CO(g),则△H=(-110.5kJ•mol-1)×2-(-393.5kJ/mol)=+172.5 kJ•mol-1,
故选B.
点评 本题考查反应热与焓变,为高频考点,把握反应的关系、盖斯定律的应用为解答的关键,侧重分析与应用能力的考查,注意利用盖斯定律计算焓变的方法,题目难度不大.


 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:选择题
| A. | 蒸馏法是海水谈化的方法之一 | |
| B. | 海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料 | |
| C. | 海水中的Li元素属于微量元素,提炼后可作Li电池原料 | |
| D. | 0℃以上,温度越高,水的密度越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度升高,Na2CO3溶液的Ksp和c(OH-)均会增大 | |
| B. | 沉淀转化的离子方程式为CO32-(aq)+CaSO4(s)?CaCO3(s)+SO42-(aq) | |
| C. | 该条件下,CaCO3的溶解度约为1×10-3g | |
| D. | CaCO3和CaSO4共存的悬浊液中,$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=9×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 I2在KI溶液中存在平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,c($I_3^-$)与温度T的平衡曲线图如图.下列说法不正确的是( )
I2在KI溶液中存在平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,c($I_3^-$)与温度T的平衡曲线图如图.下列说法不正确的是( )| A. | 反应I2(aq)+I-(aq)?I3-(aq) 的△H>0 | |
| B. | 若温度为T1、T2,反应的平衡常数分别为 K1、K2,则K1>K2 | |
| C. | 若反应进行到状态D时,一定有v正>v逆 | |
| D. | 状态A与状态B相比,状态A的c (I2) 小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol甲烷含有的电子数为NA | |
| B. | 1L0.1mol/LNa2CO3溶液中含有的CO32-数目为0.1NA | |
| C. | 1mol-OH (羟基)与l molOH-均含有10个NAe- | |
| D. | 标准状况下,2.24LCO和CO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨互为同素异形体 | |
| B. | Na的还原性强于金刚石 | |
| C. | 46g Na完全反应需要标准状况下CO2的体积为33.6L | |
| D. | 当有0.4mo1 Na参与反应时,被还原的CO2的分子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
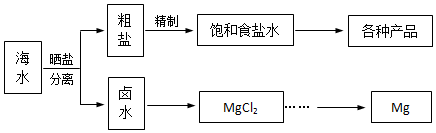
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用某有机物之间的转换可以贮存太阳能,如原降冰片二烯(NBD)经太阳光照可转化成四环烷(Q),其反应式可表示为:△H=+88.62kJ/mol下列有关说法不正确的是( )
利用某有机物之间的转换可以贮存太阳能,如原降冰片二烯(NBD)经太阳光照可转化成四环烷(Q),其反应式可表示为:△H=+88.62kJ/mol下列有关说法不正确的是( )| A. | 物质NBD比Q稳定 | |
| B. | NBD和Q互为同分异构体 | |
| C. | 物质NBD和Q的核磁共振氢谱图都有3个峰,但峰面积不同 | |
| D. | 一定条件下,1 mol NBD最多可与2 mol Br2发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com