
【题目】下表为元素周期表的粗表,①~⑧分别表示元素周期表中对应位置的元素
① | |||||||||||||||||
⑧ | ③ | ⑤ | |||||||||||||||
② | ④ | ||||||||||||||||
⑥ | |||||||||||||||||
⑦ | |||||||||||||||||
(1)用电子式表示①与②形成化合物A 的过程:________
(2)已知⑥原子的最外层有2个电子,请画出⑥原子的结构示意图:______________
(3)含有④元素的某种18 电子的离子与H+及OH-均可发生反应,请写出该离子的电子式______
(4)元素③④⑤的简单气态氢化物的稳定性由强到弱的顺序是_________(用化学式表示),其沸点由高到低的顺序是_______ (用化学式表示)
(5)已知⑦的稳定化合态为+2 价,且⑦与③可按3:4 形成某化合物,该化合物具有较强氧化性, 可以与浓盐酸反应并释放出一种黄绿色的气体, 请写出该化学方程式:_________________
(6)①与③,①与④能形成18个电子的化合物,此两种化合物在溶液中发生反应的化学方程式为_________。
(7)⑧的一种氧化物为无色气体,在空气中能迅速变成红棕色。在一定条件下,2L的该无色气体与0.5 L 的氧气混合,该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则所生成的一种含氧酸盐的化学式是_________。
(8)两种均含①与②③④四种元素的化合物相互反应放出气体的离子方程式为_________。
【答案】![]()
![]() HF>H2O>H2S H2O>HF>H2S Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O H2S+H2O2=S+H2O NaNO2 HSO3-+H+= H2O+SO2↑
HF>H2O>H2S H2O>HF>H2S Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O H2S+H2O2=S+H2O NaNO2 HSO3-+H+= H2O+SO2↑
【解析】
根据题干图表分析可知,①元素位于元素周期表的第一周期第ⅠA族,为H元素,②元素位于元素周期表的第三周期第ⅠA族,为Na元素,③元素位于元素周期表的第二周期第ⅥA族,为O元素,④元素位于元素周期表的第三周期第ⅥA族,为S元素,⑤元素位于元素周期表的第二周期第ⅦA族,为F元素,⑥元素位于元素周期表第四周期第Ⅷ族,为26号元素Fe,⑦元素位于元素周期表的第六周期第ⅣA族,为Pb元素,⑧元素位于元素周期表的第二周期第ⅤA族,为N元素,据此分析解答问题。
(1)由上述分析可知,①为H元素,②为Na元素,两者形成的化合物A为离子化合物NaH,用电子式表示其形成过程为![]() ,故答案为:
,故答案为:![]() ;
;
(2)⑥为Fe元素,核外共有26个电子,原子的最外层有2个电子,则其原子结构示意图为 ,故答案为:
,故答案为: ;
;
(3)含有S元素的某种18电子的离子与H+及OH-均可发生反应,该离子为HS-,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)非金属性越强,简单气态氢化物的稳定性越强,由于非金属性:F>O>S,则气态氢化物的稳定性:HF>H2O>H2S,因为H2O和HF分子中含有氢键,故沸点均大于H2S,且一个H2O分子中可形成两个氢键,故沸点:H2O>HF,则H2O>HF>H2S,故答案为:HF>H2O>H2S;H2O>HF>H2S;
(5)由题干已知,Pb的稳定化合态为+2价,且Pb与O可按3:4形成某化合物Pb3O4,该化合物具有较强氧化性,可以与浓盐酸反应并释放出一种黄绿色的气体Cl2,根据氧化还原反应规律可得出其化学反应方程式为:Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O,故答案为:Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O;
(6)H与O形成的18电子的化合物为H2O2,H与S形成的18电子的化合物为H2S,H2S在溶液中可被H2O2氧化生成S单质,反应方程式为H2S+H2O2=S+H2O,故答案为:H2S+H2O2=S+H2O;
(7)⑧为N元素,N的某种氧化物是一种无色气体,该气体在空气中迅速变成红棕色,则该气体为NO,2L的NO与0.5LO2相混合,该混合气体被足量NaOH溶液全吸收后没有气体残留,生成C的含氧酸盐只有一种,设含氧酸盐中N的化合价为x,根据得失电子守恒,2L×[x-(+2)]=0.5L×4,解得x=+3,所得含氧酸盐的化学式为NaNO2,故答案为:NaNO2;
(8)两种均含H、Na、O、S四种元素的化合物可相互反应放出气体,可以是硫酸氢钠与亚硫酸氢钠反应生成硫酸钠、二氧化硫和水,离子反应方程式为HSO3-+H+= H2O+SO2↑,故答案为:HSO3-+H+= H2O+SO2↑。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】反应N2(g)+O2(g)=2NO(g)的能量变化如图所示。已知:断开1mol N2(g)中化学键需吸收946kJ能量,断开1mol O2(g)中化学键需吸收498kJ能量。

下列说法正确的是
A. N2(g)+O2(g)=2NO(g) △H=-180![]()
B. NO(g)=1/2N2(g)+1/2O2(g) △H=+90![]()
C. 断开1mol NO(g)中化学键需要吸收632kJ能量
D. 形成1 mol NO(g)中化学键可释放90kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论不正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向NaHS溶液中滴入酚酞 | 溶液变红色 | HS-水解程度大于电离程度 |
B | 向浓度均为0.1mol/L的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
C | 向Na2CO3溶液中加入浓盐酸,将产生的气体通入硅酸钠溶液中 | 产生白色浑浊 | 酸性:盐酸>碳酸>硅酸 |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在I |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是( )

A. 铜片为负极,其附近的溶液变蓝,溶液中有Cu2+产生
B. 如果将锌片换成铁片,电路中的电流方向将改变
C. 其能量转化的形式主要是“化学能→电能→光能”
D. 如果将稀硫酸换成柠檬汁,LED灯将不会发光
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,FeCl2 3.0 mol/L,FeCl3 1.0 mol/L,HCl 3.0 mol/L。取废腐蚀液200 mL按如下流程在实验室进行实验:
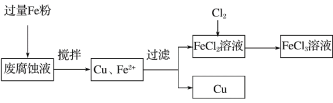
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂所需试剂是________(填化学式)。
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为__________________________________。
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。

实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是__________________________________。
(4)按上述流程操作,需称取Fe粉的质量应不少于________ g(精确到0.1 g),需通入Cl2的体积不少于________ L(标况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. ![]() 互为同系物
互为同系物
B. ![]() 的系统命名是2-甲基-1-丙醇
的系统命名是2-甲基-1-丙醇
C. 相同压强下的沸点:乙醇>乙二醇>丙烷
D. 室温下,在水中的溶解度:甘油>苯酚> 1-氯丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是硫酸试剂标签上的部分内容,据此下列说法正确的是( )

A.该硫酸试剂的物质的量浓度为18.4mol·L-1
B.该硫酸可以干燥H2S等酸性气体,但不可以干燥NH3
C.50mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46mol
D.2.7gAl与足量的该硫酸反应可得到H23.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成的。
实验目的:通过实验证明煤中含有碳元素和硫元素。
查阅资料:
(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),请完成该反应的离子方程式:___。
( )SO2+( )MnO4-+( )=( )+( )Mn2++( )
根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
实验探究:甲同学:甲同学进行了如图所示A、B两步实验:

“实验现象”:A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(2)乙同学认为甲的方案不合理,其理由是___:
实验探究:丙同学:丙同学进行了如图所示实验(部分装置在图中略去):

(3)图C装置的作用是___。
(4)证明煤中含有碳元素和硫元素的现象是:___。
(5)装置C中的高锰酸钾溶液也可以替换为___。
A.足量I2的淀粉溶液
B.足量饱和NaHCO3溶液
C.足量Na2SO3溶液
D.足量溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.1.8 g NH4+中含有的电子数为1.1NA
B.2.2 g CO2和N2O的混合气体中原子数为0.15NA
C.1 mol Na2O2与足量CO2反应,转移电子数为2NA
D.25 ℃、101 kPa时,2.24 L CH4含有的质子数为1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com