
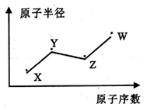
 X、Y、Z、W是四种常.见的短周期主族元素,其原子半径随原子序数的变化如图所示,己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
X、Y、Z、W是四种常.见的短周期主族元素,其原子半径随原子序数的变化如图所示,己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | B. | Y、W的最简单氢化物能相互反应 | ||
| C. | 非金属性:Z<Y | D. | X、Z、W形成的化合物均为强酸 |
分析 X、Y、Z、W是四种常见的短周期元素,Y、Z两种元素的单质是空气的主要成分,Z的原子序数大于Y,可推知Z为O、Y为N,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N元素,而原子半径小于N原子,故X为H元素,结合元素化合物性质解答.
解答 解:A.Y为N,Z为O,二者处于第二周期,W为Cl,处于第三周期,故A错误;
B.、W的最简单氢化物分别为氨气、氯化氢,能相互反应生成氯化铵,故B正确;
C.同周期元素从左到右非金属性逐渐增强,非金属性O>N,故C错误;
D.如不是最高价氧化物的水化物,如HClO,则为弱酸,故D错误.
故选B.
点评 本题考查位置结构性质关系等,为高频考点,侧重于学生的分析能力的考查,题目难度中等,推断元素是解题的关键,注意对元素周期律的理解与运用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
 爱氏试剂(由质量分数为25%盐酸、96%乙醇与无水乙醚以体积之比为1:3:1配成的混合溶液)是工商部分用于检验猪肉(含N元素)是否变质(如图)的试剂,若观察到有白烟出现,则说明猪肉已变质.下列有关说法正确的是( )
爱氏试剂(由质量分数为25%盐酸、96%乙醇与无水乙醚以体积之比为1:3:1配成的混合溶液)是工商部分用于检验猪肉(含N元素)是否变质(如图)的试剂,若观察到有白烟出现,则说明猪肉已变质.下列有关说法正确的是( )| A. | 白烟的成分为NH4Cl | |
| B. | 可用稀硫酸代替盐酸 | |
| C. | 腐败肉样释放出的是N2 | |
| D. | 该检验可直接将肉样放入爱氏试剂中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用纯铜作阳极、粗铜作阴极 | |
| B. | 电解液的成分保持不变 | |
| C. | 屯解过程中,阳极质量的减少与阴明极质量的增加相等 | |
| D. | 阴极电极反应为:Cu2++2e-=Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上,采用电解MgCl2溶液的方法制取金属镁 | |
| B. | 利用太阳能等淸洁能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 硬币材质一般都是合金,所有的不锈钢中都含有非金属元素 | |
| D. | 使用含钙、镁离子浓度较大的地下水洗衣服,肥皂去污能力会减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu 溶于稀 HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用CH3COOH溶解 CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | FeCl3溶液与Cu反应:2Fe3++Cu═2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 漂白粉的成分为次氯酸钙和氯化钙 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 实验室可用NaOH溶液处理NO2和HCl废气 | |
| D. | 浓硫酸具有强氧化性,所以浓硫酸可用于干燥H2和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com