
 ��
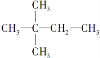
�� ��˵�������к���1��C=C������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã��ݴ�ȷ��A�Ľṹ��ʽ������A��2��̼ԭ�ӵ�ͬϵ�����ʽΪC4H8�������ʿ���������ϩ���춡ϩ��
��˵�������к���1��C=C������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã��ݴ�ȷ��A�Ľṹ��ʽ������A��2��̼ԭ�ӵ�ͬϵ�����ʽΪC4H8�������ʿ���������ϩ���춡ϩ��
| ||
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ��
�� ��˵�������к���1��C=C������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã���A�Ľṹ��ʽΪ����CH3��3CCH=CH2��CH2=C��CH3��CH��CH3��2 ��
��˵�������к���1��C=C������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã���A�Ľṹ��ʽΪ����CH3��3CCH=CH2��CH2=C��CH3��CH��CH3��2 ��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�23 g NO2 ����NA����ԭ�� |
| B�����³�ѹ�£�Na2O2������H2O��Ӧ��������0.1 mol O2��ת�Ƶ��ӵ���ĿΪ0.4NA |
| C�����³�ѹ�£�22.4 L CCl4 ����NA��CCl4 ���� |
| D��1 mol Fe2+�������� H2O2 ��Һ��Ӧ��ת�� 2NA ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ӡˢ��·�����Ȼ�����Һ��ʴͭ��Fe3++Cu=Fe2++Cu2+ |
| B����С�մ�������ͷ��CH3CH��OH��COOH+HCO3-=CO2��+H2O+CH3CH��OH��COO- |
| C������Na2SO3������뵽��������ˮ�У�SO32-+Cl2+2OH-=SO42-+2Cl-+H2O |
| D���ù���ʯ��ˮ��Ӳˮ������Mg2++2HCO3-+Ca2++2OH-�TCaCO3��+2H2O+MgCO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������Ĵ����ƾ�������pH����������pH���� |
| B���¶����ߣ�����Һ��pH������ |
| C��������Һ��ˮ�ĵ��붼�����ƣ���ˮ�ĵ���̶���� |
| D�����������п����������������һ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ͷ��� |
| B�������3-�һ����� |
| C�������3-������ |
| D�������2-������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com