

| A. | 反应表明拆开N-C键比N-N键容易 | B. | 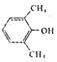 属于芳香醇的异构体有5种 属于芳香醇的异构体有5种 | ||
| C. | PHAC是一种酸式盐 | D. | PHAC能用于制造高能炸药 |
分析 A.根据图知,该反应中需要催化剂、氧化剂使C-N键转化为N-N键;
B. 属于芳香醇的同分异构体中可能含有取代基-CH3和-CH2OH、-CH2CH2OH、-CH(CH3)OH、CH;
属于芳香醇的同分异构体中可能含有取代基-CH3和-CH2OH、-CH2CH2OH、-CH(CH3)OH、CH;
C.该化合物中含有水合氢离子;
D.PHAC属于含能材料,PHAC分解温度高达116.8℃,具有非常好的热稳定性.
解答 解:A.根据图知,该反应中需要催化剂、氧化剂使C-N键转化为N-N键,所以说明拆开N-C键比N-N键困难,故A错误;
B. 属于芳香醇的同分异构体中可能含有取代基-CH3和-CH2OH,有3种符合条件的同分异构体;含有-CH2CH2OH有一种同分异构体,含有-CH(CH3)OH有一种同分异构体,所以符合条件的有5种同分异构体,故B正确;
属于芳香醇的同分异构体中可能含有取代基-CH3和-CH2OH,有3种符合条件的同分异构体;含有-CH2CH2OH有一种同分异构体,含有-CH(CH3)OH有一种同分异构体,所以符合条件的有5种同分异构体,故B正确;
C.该化合物中含有水合氢离子,所以属于酸式盐,故C正确;
D.PHAC属于含能材料,PHAC分解温度高达116.8℃,具有非常好的热稳定性,所以PHAC能用于制造高能炸药,故D正确;
故选A.
点评 本题考查有机物结构和性质,为高频考点,明确基本概念、同分异构体种类判断方法是解本题关键,侧重考查学生理解、判断及知识综合运用能力,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种溶液中pH最小的是① | |
| B. | 3种溶液中水的电离程度最大的是② | |
| C. | ①与②等体积混合后溶液显酸性 | |
| D. | ①与③等体积混合后c(H+)>c(CH3COO-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和溴水共热生成溴苯 | |
| B. | 2,2-二甲基丙烷是正戊烷的同系物 | |
| C. | 乙醇、正戊烷、苯均可通过石油的分馏得到 | |
| D. | 乙醇、正戊烷、苯均能发生取代反应和氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeC13溶液中滴加HI解液:2Fe3++2HI═2Fe2++2H++I2 | |
| B. | 1mol•L-1NaA1O2溶液和4 mol•L-1HCl溶液等体积混合:AlO2++4H+═Al3++2H2O | |
| C. | NH4HSO4溶液中滴加少量Ba(OH)2溶液:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O | |
| D. | Na2S2O3溶液中滴加过量稀H2SO4:3S2O32-+2H+═4S↓+2SO42-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氰化钾中含有离子键和极性键 | |
| B. | 氰化钾中碳元素的化合价为+4价 | |
| C. | KCN与KMnO4溶液反应可能生成CO2和N2 | |
| D. | 相同条件下,KCN溶液的碱性强于CH3COOK溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com