
| A. | SO2是形成酸雨的主要气体 | |
| B. | 用碱液吸收燃煤废气可减少环境污染 | |
| C. | 用水溶解、过滤除去煤中的单质硫以减少SO2排放 | |
| D. | 往燃煤中混入生石灰,可减少SO2排放 |
科目:高中化学 来源: 题型:选择题
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:ClO-+CO2+H2O=HClO+HCO3- | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ | |
| C. | 从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- | |
| D. | Ca(ClO)2溶液中通入过量的SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaCl溶液中滴入AgNO3溶液有沉淀 | |
| B. | 同一钢笔同时使用不同牌号的墨水易发生堵塞 | |
| C. | 在河流入海口易形成三角洲 | |
| D. | 在实验中不慎手被玻璃划破,可用FeCl3溶液应急止血 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
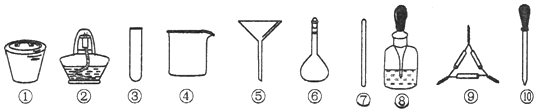
| A. | 将海带剪碎后灼烧成灰,选用①、②和⑨ | |
| B. | 将海带灰加蒸馏水溶解,选用④、⑥和⑦ | |
| C. | 过滤得到滤液,选用④、⑤和⑦ | |
| D. | 取滤液,先加入几滴稀硫酸,再滴加H2O2,最后滴加淀粉溶液,选用③和⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol NH3 | B. | 标准状况下22.4L He | ||
| C. | 100ml 10%的食盐水 | D. | 147g H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c1=2c2 | B. | c2=2cl | C. | c2>2c1 | D. | c2<2cl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
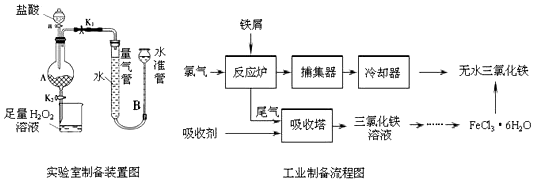
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com