
| A. | 1.4g | B. | 2.8g | C. | 5.6g | D. | 11.2g |
分析 铁粉放入三氯化铁溶液中发生反应Fe+2Fe3+=3Fe2+,根据n=cV计算出原溶液中Fe3+的物质的量,根据方程式计算生成的Fe2+的物质的量,进而得到未反应的Fe3+的物质的量,然后根据铁离子和亚铁离子的浓度相同列式计算出铁片减少的物质的量,最后根据m=nM计算出铁片减少的质量.
解答 解:1L0.5mol/L的氯化铁溶液中含有氯化铁的物质的量为:0.5mol/L×1L=0.5mol,
设参加反应的铁为xmol,则:
Fe+2Fe3+=3Fe2+
xmol 2xmol 3xmol
溶液中的Fe3+和Fe2+浓度相等,则:0.5mol-2x=3x,解得:x=0.1mol,
所以铁片减少的质量为:0.1mol×56g/mol=5.6g,
故选C.
点评 本题考查氧化还原反应的计算,侧重于学生的分析能力和计算能力的考查,为高频考点,题目难度不大,明确发生反应的实质为解答关键.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:选择题
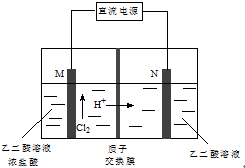 乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法正确的是( )| A. | M极与直流电源的负极相连 | |
| B. | 若有2 molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol | |
| C. | N电极上的电极反应式:HOOC-COOH-2e-+2H+=HOOC-CHO+H2O | |
| D. | 乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O=HOOC-CHO+2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液 | B. | BaCl2溶液 | C. | Ba(OH)2溶液 | D. | Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
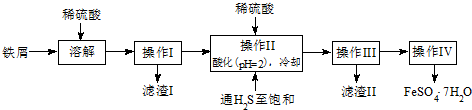
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 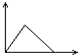 | C. | 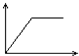 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、[Al(OH)4]-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO${\;}_{3}^{-}$ | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 品红溶液:红色褪去,加热该褪色溶液,仍无色:氯气具有漂白性 | |
| B. | 紫色石蕊溶液:先变红,后褪色;氯气与水反应生成盐酸和次氯酸 | |
| C. | 含酚酞的氢氧化钠溶液:红色褪去;氯气只作氧化剂 | |
| D. | 硫化钠溶液:溶液变浑浊;氯气只作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com